La Expresión Génica y la Epigenética: Cómo la Dieta y el Entorno Determinan su Salud
Lo importante no son los genes, sino la forma en que se expresan.
Milos Pokimica
Escrito por: Milos Pokimica
Revisado Médicamente Por: Dr. Xiùying Wáng, M.D.
Updated enero 5, 2026Principales Conclusiones:
-La expresión génica y la epigenética son procesos dinámicos y reactivos que regulan cómo se activan o desactivan los genes en respuesta a diversos estímulos.
-La dieta y el medio ambiente son dos factores importantes que pueden influir en la expresión génica y la epigenética, al proporcionar nutrientes, sustancias químicas o señales que pueden modificar el ADN o las proteínas que interactúan con él.
- Los cambios en la expresión génica pueden tener efectos significativos sobre la salud y la prevención de enfermedades, al alterar las funciones celulares, el metabolismo, la inflamación, la inmunidad y el envejecimiento del organismo.
Introducción.
La mayoría de la gente está familiarizada hasta cierto punto con la ciencia que hay detrás de la genética. Genética nos ayuda a entender cómo funciona la evolución y cómo heredamos rasgos de nuestros padres y nos ayuda en medicina, o antropología comprendiendo cómo evolucionaron nuestros cuerpos desde los homínidos hasta los humanos anatómicamente modernos.
Pero ¿qué pasa con epigenética? ¿Está familiarizado con este término? ¿Sabe que los genes no están grabados en piedra? ¿Sabe cómo podemos cambiar nuestro destino influyendo en nuestros genes? La epigenética es un campo científico nuevo y emergente.
Genética clásica.
Pero, ¿cómo hemos llegado hasta aquí? ¿Cómo hemos descubierto los secretos del ADN y los mecanismos que lo regulan?
Todo empezó con un monje llamado Gregor Mendel, que vivió en el siglo XIX. Tenía curiosidad por saber cómo heredaban las plantas rasgos como el color de las flores y la forma de las semillas. Hizo experimentos con plantas de guisantes, cruzándolas y contando la descendencia. Observó que algunos rasgos seguían patrones simples de herencia, mientras que otros parecían mezclarse o desaparecer. Elaboró unas reglas que explicaban sus observaciones y que hoy conocemos como las leyes de Mendel sobre la herencia. Publicó su trabajo en 1865, pero a nadie le interesó. Murió sin saber que era el padre del campo más importante de la ciencia llamado genética.
A principios del siglo XX. Algunos científicos redescubrieron el trabajo de Mendel y se dieron cuenta de que era genial. También descubrieron que los cromosomas estaban formados por ADN y proteínas y que portaban las unidades de la herencia, a las que llamaron genes. Averiguaron cómo estaban dispuestos los genes en los cromosomas, cómo podían intercambiarse durante la meiosis (división celular) y cómo podían mutar por radiación o sustancias químicas. También aprendieron a cartografiar los genes en los cromosomas utilizando el análisis de ligamiento y las frecuencias de recombinación. Era la época de la genética clásica.
Pero había un problema. La genética clásica no podía explicarlo todo. Por ejemplo, ¿cómo controlaban los genes los rasgos? ¿Cómo interactuaban los genes con el medio ambiente o qué efecto tenía éste en nuestro genoma? ¿Cómo cambiaban los genes con el tiempo y entre generaciones? Estas preguntas condujeron a la creación de una nueva disciplina denominada biología molecular.
Dogma central.
En 1953 James Watson y Francis Crick resolvieron el estructura del ADN. Se trataba de una doble hélice formada por cuatro nucleótidos (A, T, C, G) que se emparejaban entre sí de una forma específica (A con T, C con G). Se dieron cuenta de que esta estructura explicaba cómo el ADN podía almacenar información (la secuencia de nucleótidos), copiarse a sí mismo (separando las hebras y utilizándolas como plantillas) y expresarse (transcribiéndose en ARN y traduciéndose en proteínas). Este trabajo se convirtió en el "dogma central de la biología molecular". Una teoría afirma que la información genética fluye sólo en una dirección, del ADN, al ARN, a la proteína, o del ARN directamente a la proteína. Fue enunciada por primera vez por Francis Crick en 1957 y publicada en 1958.
Pero había otro problema. La biología molecular tampoco podía explicarlo todo.
Por ejemplo, ¿cómo saben las células cuándo y dónde activar y desactivar los genes? Durante el desarrollo, ¿cómo se dividen las células en distintos tipos porque todas tienen el mismo ADN? ¿Cómo recuerdan las células su identidad y su historia, algo importante para la investigación del cáncer? ¿Cómo responden las células a las señales de otras células o del entorno?
Nacimiento de la epigenética.
Estas preguntas condujeron al nacimiento de la epigenética, cuyo objetivo era desvelar los mecanismos que regulan la expresión de los genes sin cambiar la secuencia del ADN.
El término epigenética fue acuñado por Conrad Waddington en 1942, pero tardó décadas en ganar aceptación científica.
La epigenética se basa en la idea de que existen modificaciones químicas en el ADN o en histonas (proteínas que envuelven el ADN) que pueden afectar al modo en que la maquinaria celular accede a los genes y los utiliza. Estas modificaciones pueden ser añadidas o eliminadas por enzimas, dependiendo de diversos factores como el tipo de célula, la fase de desarrollo, las señales ambientales, el estrés, la dieta, etc. (Peixoto et al., 2020). Estos cambios también pueden transmitirse a las células hijas durante la división celular, o incluso a los hijos durante la reproducción.
Esto significa que la epigenética puede influir en rasgos que no están codificados únicamente por el ADN, como el comportamiento, la propensión a enfermedades o el envejecimiento.
La epigenética es uno de los temas más candentes, tanto como lo fue en su día la genética. El problema es que la mayoría de la gente no ha oído hablar de ella, por lo que persiste la vieja creencia de que los genes lo son todo. Tenemos que divulgar las nuevas investigaciones entre un público más amplio que sigue creyendo que los genes están grabados en piedra y que no se puede hacer nada al respecto. La epigenética pone en tela de juicio algunos de los supuestos y dogmas de la genética y la biología molecular. Abre nuevas posibilidades para comprender la vida a un nivel más profundo. También abre nuevas vías para mejorar la medicina y la salud modificando la expresión de los genes.
Lo importante no son los genes, sino la forma en que se expresan.
¿Qué es la expresión génica?
Antes de adentrarnos más científicamente en la epigenética, hablemos de la expresión génica.
La expresión génica se refiere a la frecuencia o el momento en que se crean proteínas a partir de las instrucciones contenidas en los genes. (What Is Epigenetics? | CDC, 2022b).
Las proteínas son los bloques de construcción. Desempeñan muchas funciones, como la construcción de tejidos, la lucha contra las infecciones y la regulación de las hormonas (Pelusa et al., 2022).
Los genes contienen la información necesaria para producir proteínas, pero no las producen por sí mismos. Necesitan la ayuda de otras moléculas, como ARN y enzimas, para leer el código y producir las proteínas. Este proceso se denomina transcripción (Blackwell et al., 2006).
La transcripción no siempre está activada. Puede activarse o desactivarse en función de distintos factores, como señales de otras células, hormonas o nutrientes. Así es como nuestro organismo se adapta a las distintas situaciones.
Por ejemplo, cuando tienes hambre, tu cuerpo activa genes que hacen que las enzimas descompongan los alimentos y liberen energía. Cuando estás lleno, el cuerpo desactiva esos genes y activa los que almacenan el exceso de energía en forma de grasa.
¿Por qué es importante la epigenética?
Epi significa "por encima de" en griego. Lo importante no son los genes, sino lo que expresan.
Todas sus células tienen los mismos genes, pero tienen un aspecto y actúan de forma diferente debido a los cambios epigenéticos. En otras palabras, se trata de una capa adicional de información que controla la regulación de los genes (Hamilton et al., 2011).
Las modificaciones epigenéticas pueden inhibir o activar la expresión génica. Una combinación de estas modificaciones desempeña un papel importante en la "impronta", un tipo de "marca" que determina si un gen se expresará o no.
El ADN está formado por combinaciones de nucleótidos. Estas son las famosas letras que la mayoría de la gente conoce: adenina (A), tiamina (T), guanina (G) y citosina (C).
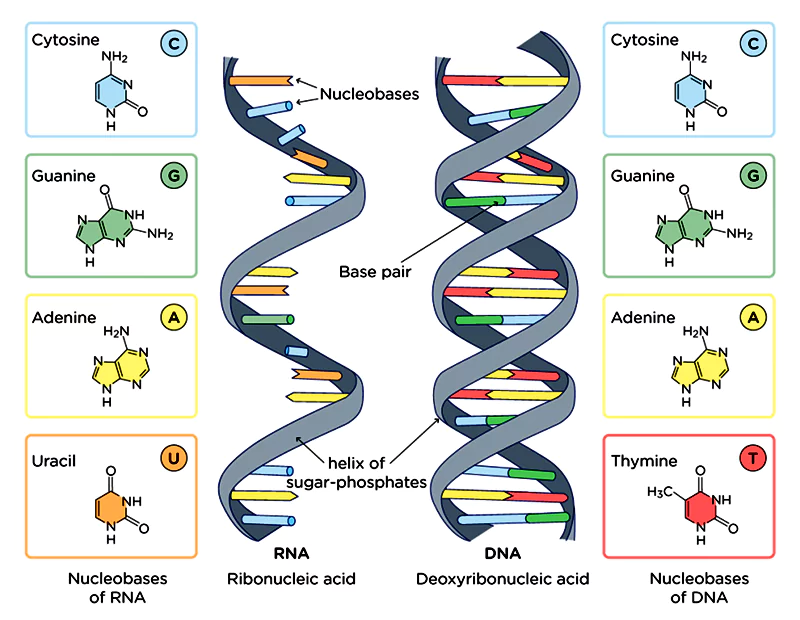
La citosina, por ejemplo, puede modificarse añadiendo un grupo metilo (CH3).
Este proceso se conoce como metilación, y altera la expresión del gen cuya secuencia ha sido alterada. La metilación del ADN suele provocar el silenciamiento del gen. En las circunstancias equivocadas, esto podría ser muy malo si el gen regula la función inmunitaria o alguna otra función importante.
Los cambios epigenéticos pueden producirse incluso antes de nacer, durante el desarrollo y a lo largo de la vida. Algunos cambios epigenéticos son normales y necesarios para tu crecimiento y funcionamiento.
Otros cambios epigenéticos están influidos por el comportamiento y el entorno.
Por ejemplo, lo que come puede afectar a la metilación de sus genes o a la modificación de sus histonas.
Su actividad física puede afectar a la cantidad de ARN no codificante que se produce o a su interacción con el ARN codificante.
Estos cambios epigenéticos forman parte de la evolución y tienen su razón de ser, pero también pueden tener efectos positivos o negativos en la salud.
Algunos cambios epigenéticos, por ejemplo, pueden mejorar nuestro sistema inmunitario activando genes que combaten la inflamación o el cáncer.
Otros cambios epigenéticos pueden aumentar el riesgo de enfermedades al desactivar genes que regulan el metabolismo o el sistema inmunitario (Fanucchi et al, 2021); (Surace et al., 2019).
Esta es una fuerza motriz de la adaptación y la evolución. Si quiere una prueba de la evolución y de cómo funciona en tiempo real y cómo evolucionan los organismos, es ésta. Esta es la razón por la que los cambios epigenéticos también pueden heredarse de una generación a otra. Por ejemplo, si sus abuelos estuvieron expuestos a toxinas, mutágenos o factores estresantes y esa exposición provocó cambios epigenéticos en su ADN o en sus espermatozoides u óvulos, esos cambios podrían transmitirse a usted y afectar a su expresión génica (Denhardt et al., 2018).
Tener un entorno contaminado y toxinas por todas partes no sólo afectará a tu ADN, sino también al de tus hijos (de Magalhães-Barbosa et al., 2022).
Cambios epigenéticos y sus efectos en la salud.
La siguiente tabla ilustra los principales factores que influyen en la expresión génica y los cambios epigenéticos. Hay más factores, pero lo que puede llevarse a casa de esta tabla es el hecho de que en cada fila los factores que influyen en el riesgo son la dieta, el estrés y la exposición a toxinas.
| Cambios epigenéticos | Efectos sobre la salud | Fuentes |
| Metilación del ADN | Proceso que añade grupos metilo a las bases del ADN, lo que afecta a la expresión de los genes. Variables ambientales como la alimentación, el estrés y exposición a la toxicidad pueden alterar la metilación del ADN. La metilación del ADN puede afectar a diversos aspectos de la salud, como el riesgo de cáncer, la función inmunitaria y el envejecimiento. | Cavalli et al., 2019 |
| Modificaciones de las histonas | Proceso que altera la estructura de las histonas, las proteínas que envuelven el ADN. Las modificaciones de las histonas pueden afectar al empaquetamiento del ADN, afectando a la expresión génica. Las modificaciones de las histonas pueden verse influidas por factores ambientales como la dieta, el estrés y la exposición a toxinas. Las modificaciones de las histonas pueden afectar a varios aspectos de la salud, como el riesgo de cáncer, la función inmunitaria y el envejecimiento. | Cavalli et al., 2019 |
| ARN no codificante | ARN que no codifica proteínas. Factores ambientales como la dieta, el estrés y la exposición a toxinas pueden afectar al ARN no codificante. El ARN no codificante puede influir en muchos aspectos de la salud, como el riesgo de cáncer, la función inmunológica y el envejecimiento. | Cavalli et al., 2019 |
| Infecciones | Los gérmenes pueden cambiar tu epigenética para debilitar tu sistema inmunitario. Esto ayuda al germen a sobrevivir. Por ejemplo: Mycobacterium tuberculosis causa la tuberculosis. La tuberculosis era y aún puede ser una enfermedad mortal porque puede alterar la metilación del ADN de las células inmunitarias, haciendo así que el sistema inmunitario sea menos eficaz para combatir la infección. | What Is Epigenetics? | CDC, 2022b |
Ejemplos de cambios epigenéticos y sus efectos en el riesgo de cáncer.
El cáncer es una enfermedad compleja en la que intervienen miles de mutaciones diferentes que se van acumulando y que implica tanto cambios en el genoma como en el epigenoma (Brena et al., 2007), (Shen et al., 2013). Puedes tener una predisposición genética a que te den miedo tus padres, pero eso es sólo una parte de todo el cuadro.
Esa predisposición genética al cáncer en realidad se activa dependiendo de la expresión de los genes y la expresión de los genes depende sobre todo de una dieta (Hullar et al., 2014), y medio ambiente (Abdul et al., 2017).
Los cambios epigenéticos pueden activar o desactivar genes implicados en el crecimiento celular, la muerte celular o la respuesta inmunitaria. Estos cambios pueden afectar al riesgo general de desarrollar cáncer o de responder a su tratamiento. Por eso tenemos una epidemia de cáncer en la que una de cada cuatro personas en las sociedades occidentales con una dieta americana estándar morirán de ello. La causa no son los genes malos, sino la expresión genética.
He aquí algunos ejemplos de cambios epigenéticos y sus efectos sobre el riesgo de cáncer:
- La metilación del ADN impide que las proteínas que leen el gen accedan a él, lo que básicamente lo desactiva. La metilación del ADN puede desactivar genes que suprimen tumores o reparan daños en el ADN, lo que básicamente desactiva el sistema inmunitario. Por ejemplo, tener una mutación en el gen BRCA1 que impide que funcione correctamente aumenta la probabilidad de padecer cáncer de mama y otros tipos de cáncer. Sin embargo, si este gen también está metilado, lo más probable es que usted muera porque su sistema inmunitario está desactivado. La metilación puede aumentar aún más el riesgo de cáncer y hacerlo más agresivo (Catteau et al., 2002), (Prajzendanc et al., 2020).
- La modificación de las histonas se produce cuando se añaden o eliminan grupos químicos de las histonas, unas proteínas que envuelven el ADN para formar una estructura llamada cromatina. Dependiendo del tipo y la ubicación de los grupos químicos, la modificación de las histonas puede hacer que la cromatina esté más apretada o menos apretada, afectando a la cantidad de ADN que queda expuesto u oculto a las proteínas que lo leen. La modificación de las histonas puede afectar a los genes que regulan el ciclo celular, Por ejemplo, tener una mutación en el gen p53 que le impida funcionar correctamente le hace más propenso a padecer diversos tipos de cáncer. Sin embargo, si este gen también está modificado por histonas, puede aumentar aún más su riesgo de cáncer o hacer que su cáncer sea más resistente al tratamiento (Yue et al., 2017).
- ARN no codificante: Se produce cuando unas moléculas denominadas ARN no codificante se unen al ARN codificante, que se utiliza para fabricar proteínas. El ARN no codificante puede ayudar a descomponer el ARN codificante o reclutar moléculas que modifican las histonas, afectando a la expresión génica. El ARN no codificante puede afectar a genes que controlan la diferenciación celular, la invasión o la metástasis. Por ejemplo, tener una mutación en el gen KRAS que impida su correcto funcionamiento aumenta la probabilidad de padecer cáncer colorrectal. Sin embargo, si este gen también está regulado por ARN no codificante, puede aumentar aún más su riesgo de cáncer o hacer que su cáncer sea más difícil de tratar (Saliani et al., 2022).
Cambios epigenéticos y sus efectos en función de la dieta y la nutrición
| Componentes de la dieta | Cambios epigenéticos | Fuentes |
| Antioxidantes | Los antioxidantes son moléculas capaces de neutralizar los radicales libresque pueden dañar el ADN y las histonas. Los antioxidantes pueden modular los cambios epigenéticos afectando a la metilación del ADN y a las modificaciones de las histonas. | Beetch et al., 2020 |
| Folato | El folato es una vitamina B que interviene en la síntesis del ADN y el ARN. El folato puede afectar a los cambios epigenéticos al proporcionar grupos metilo para la metilación del ADN. La deficiencia de folato puede alterar la metilación del ADN y aumentar el riesgo de diversas enfermedades, como el cáncer, los defectos del tubo neural y el deterioro cognitivo. | Crider et al., 2012 |
| Restricción calórica | La restricción calórica es una intervención dietética que reduce la ingesta de calorías sin causar desnutrición mediante la regulación a la baja de diversos factores, como la inflamación, el estrés oxidativo y la tasa metabólica basal. La restricción calórica puede afectar a los cambios epigenéticos al alterar la expresión y la actividad de las enzimas implicadas en la metilación del ADN y las modificaciones de las histonas. | Gensous et al., 2019 |
| Fibra | La fibra es un tipo de carbohidrato que no es digerido por las enzimas humanas pero que puede ser fermentado por las bacterias intestinales. La fibra puede afectar a los cambios epigenéticos al influir en la composición y función de la microbiota intestinal, que puede producir metabolitos que modulan la metilación del ADN y las modificaciones de las histonas. | Choi et al., 2010 |
| Probióticos | Los probióticos pueden afectar a los cambios epigenéticos al influir en la composición y función de la microbiota intestinal, que puede producir metabolitos que modulen la metilación del ADN y las modificaciones de las histonas. Los probióticos también pueden modular la expresión de genes implicados en la inflamación, la inmunidad y el metabolismo. | (Borzabadi et al., 2018), (Ye et al., 2017) |
| Prebióticos | Los prebióticos son hidratos de carbono no digeribles que estimulan selectivamente el crecimiento y/o la actividad de las bacterias intestinales beneficiosas. Los prebióticos pueden afectar a los cambios epigenéticos al influir en la composición y función de la microbiota intestinal, que puede producir metabolitos que modulan la metilación del ADN y las modificaciones de las histonas. Los prebióticos también pueden modular la expresión de genes implicados en la inflamación, la inmunidad y el metabolismo. | Ye et al., 2017 |
Efecto de los antioxidantes en la expresión génica.
He aquí algunos ejemplos. No se trata de una lista completa de todos los efectos, sólo de un ejemplo:
- Los antioxidantes pueden prevenir o invertir la metilación del ADN. La metilación del ADN puede producirse al exponerse a radicales libres o toxinas. Los antioxidantes pueden bloquear este proceso o eliminar el grupo metilo, restaurando la función del gen.
- Los antioxidantes pueden modular las modificaciones de las histonas. Los antioxidantes pueden influir en las enzimas que realizan estas modificaciones, cambiando la estructura de la cromatina.
- Los antioxidantes pueden regular el ARN no codificante. Los antioxidantes pueden afectar a la producción o actividad del ARN no codificante, alterando la regulación génica.
- Los antioxidantes pueden prevenir o reparar daños en el ADN y restablecer la expresión normal de los genes, evitando o ralentizando el desarrollo del cáncer.
En la tabla siguiente se muestran antioxidantes seleccionados y sus efectos sobre la expresión génica. No es una lista completa, sólo algunos ejemplos que han sido investigados por los científicos. Existen miles de fitoquímicos diferentes y debería o no ser capaz de investigarlos todos. Debe esforzarse por aumentar la valor ORAC global de su dieta a través de la nutrición y no seguir la ruta de los antioxidantes suplementarios individuales. Los fitoquímicos actúan de forma sinérgica como un complejo de sustancias químicas procedentes de fuentes de alimentos integrales, donde 2 más 2 es igual a 15. En la tabla, he enumerado algunos antioxidantes sólo como ejemplo.
| Antioxidante | Efecto sobre la epigenética | Fuente |
| Curcumina | La curcumina es un polifenol antiinflamatorio, antioxidante y anticancerígeno producido a partir de la cúrcuma. La curcumina puede inhibir las metiltransferasas de ADN (DNMT) y las desacetilasas de histonas (HDAC), provocando la reactivación de genes supresores de tumores y la supresión de oncogenes. La curcumina también puede modificar la estructura de la cromatina y la expresión de los genes al inducir la acetilación y metilación de las histonas. La curcumina puede modular los microARN (miARN) y los ARN no codificantes largos (lncARN), ambos dirigidos a genes implicados en la inflamación, la apoptosis, el ciclo celular, la invasión y la metástasis. | Bhattacharjee et al., 2020 |
| Resveratrol | El resveratrol es un polifenol natural que se encuentra en las uvas, el vino tinto, las bayas y los cacahuetes y tiene efectos antioxidantes, antiinflamatorios y anticancerígenos. El resveratrol puede inhibir las DNMT y las HDAC, lo que provoca la desmetilación y reactivación de genes supresores de tumores y la regulación a la baja de oncogenes. El resveratrol también puede inducir la acetilación y metilación de histonas, lo que afecta a la estructura de la cromatina y la expresión génica. El resveratrol puede regular miRNAs y lncRNAs que se dirigen a genes implicados en el estrés oxidativo, la inflamación, la apoptosis, la autofagia, la senescencia, la angiogénesis y la metástasis. | Griñán-Ferré et al., 2020 |
| Apigenina | La apigenina es un flavonoide natural derivado de las flores de manzanilla, las naranjas, el perejil, el apio y otras fuentes naturales que tiene propiedades antioxidantes, antiinflamatorias y anticancerígenas. La apigenina puede inhibir las DNMT y las HDAC, lo que provoca la desmetilación y reactivación de genes supresores de tumores y la regulación a la baja de oncogenes. La apigenina también puede inducir la acetilación y metilación de histonas, alterando la estructura de la cromatina y la expresión génica. La apigenina puede regular los miARN que se dirigen a genes implicados en el ciclo celular, la apoptosis, la invasión, la metástasis, la angiogénesis y el tallo. | Bhattacharjee et al., 2020 |
| Sulforafano | El sulforafano es un isotiocianato natural derivado de las verduras crucíferas como el brócoli, El sulforafano es un antioxidante, antiinflamatorio y anticancerígeno. El sulforafano puede inhibir las DNMT y las HDAC, lo que provoca la desmetilación y reactivación de genes supresores de tumores y la regulación a la baja de oncogenes. El sulforafano también puede inducir la acetilación y metilación de histonas, alterando la estructura de la cromatina y la expresión génica. El sulforafano puede regular los miARN y los lncARN que se dirigen a genes implicados en la inflamación, la apoptosis, el ciclo celular, la invasión y la metástasis. | Bhattacharjee et al., 2020 |
| Ácido ursólico | El ácido ursólico es un triterpenoide pentacíclico natural que se encuentra en varias frutas, hierbas y especias y tiene efectos antioxidantes, antiinflamatorios y anticancerígenos. El ácido ursólico puede inhibir las DNMT y las HDAC, lo que provoca la desmetilación y reactivación de genes supresores de tumores y la regulación a la baja de oncogenes. El ácido ursólico también puede inducir la acetilación y metilación de histonas, afectando a la estructura de la cromatina y a la expresión génica. El ácido ursólico puede regular los miARN que se dirigen a genes implicados en el ciclo celular, la apoptosis, la invasión, la metástasis, la angiogénesis y el tallo. | Bhattacharjee et al., 2020 |
| Allicina | La alicina es un compuesto natural de azufre derivado de ajo que tiene efectos antimicrobianos, antioxidantes, antiinflamatorios y anticancerígenos. La alicina puede inhibir la actividad de la ADN girasa en las bacterias, lo que provoca la inhibición de la replicación y la transcripción del ADN. La alicina también puede oxidar los residuos de cisteína de las proteínas, afectando a su estructura y función. La alicina puede regular los miARN dirigidos a genes implicados en el ciclo celular, la apoptosis, la invasión, la metástasis, la angiogénesis y el crecimiento. | Chhabria et al., 2015 |
Hay muchos más antioxidantes que pueden afectar a la expresión génica. Si quiere saber más, puede buscar artículos correlacionados.
Es posible que también se pregunte de dónde puede obtener antioxidantes. La buena noticia es que se encuentran sobre todo en las plantas y que hay plantas muy ricas en contenido antioxidante. Conozca sus valores ORAC.
Efectos del folato en la expresión génica.
El folato es una vitamina B que interviene en la síntesis de ADN y ARN. El folato es necesario para que las células crezcan y se dividan correctamente. Puedes obtener folato de alimentos como las verduras de hoja verde, las judías, los frutos secos, los huevos y los cereales enriquecidos. El problema es que éste es uno de los deficiencias en la dieta estadounidense estándar. Las personas que siguen una dieta integral a base de plantas no suelen tener carencias de folato y no necesitan un suplemento adicional de ácido fólico.
He aquí algunos ejemplos:
- El folato proporciona grupos metilo (un grupo de carbono) para la metilación del ADN (Crider et al., 2012). El folato es una de las principales fuentes de grupos metilo para este proceso. La carencia de folato puede alterar la metilación del ADN y provocar una expresión génica anormal.
- El folato afecta al cierre del tubo neural. El tubo neural es la estructura que forma el cerebro y la médula espinal en el embrión. El tubo neural necesita cerrarse correctamente para un desarrollo normal. El folato es esencial para este proceso porque afecta a la expresión de los genes implicados en el cierre del tubo neural (Saitsu et al., 2017). La carencia de folato puede impedir el cierre del tubo neural y causar defectos congénitos como la espina bífida.
- El folato es importante para la función cognitiva porque afecta a la expresión de genes implicados en el desarrollo y la función cerebrales. La carencia de folato puede deteriorar la función cognitiva y aumentar el riesgo de demencia.
Estos son algunos de los efectos del folato en la epigenética y por qué son importantes para tu salud y desarrollo. Quizá te preguntes cuánto folato necesitas y de dónde puedes obtenerlo. Aquí tienes algunos consejos:
- La CDR de folato es de 400 microgramos para los adultos y de 600 mcg para las mujeres embarazadas.
- Puedes obtener folato de alimentos como las verduras de hoja verde, las judías, los frutos secos, los huevos y los cereales enriquecidos. También puedes tomar un suplemento si tienes una deficiencia o una mayor necesidad de folato.
- Hay que evitar tomar demasiado folato porque puede enmascarar una vitamina deficiencia de vitamina B12 o interferir con algunos medicamentos.
- o interferir con algunos medicamentos. Necesitamos folato pero los suplementos están hechos de ácido fólico. Nuestro hígado, a diferencia del hígado de las ratas en el modelo animal, es incapaz de convertir más de 400mg de ácido fólico en folato en un día. Por eso la mayoría de los suplementos nunca superan los 400mg de ácido fólico.
Efectos de la restricción calórica en la expresión génica.
La restricción calórica consiste en reducir la ingesta de calorías sin provocar desnutrición. La restricción calórica puede afectar a la cantidad de ARN no codificante que se produce o a su interacción con el ARN codificante (Abraham et all., 2017). La restricción calórica también puede regular el ritmo circadiano de la expresión génica en diferentes órganos y tejidos (Patel et al., 2016).
Estos efectos de la restricción calórica sobre la epigenética pueden tener diversos beneficios para la salud y el envejecimiento. Por ejemplo:
- La restricción calórica puede retrasar el envejecimiento modulando diversas vías, como la inflamación (Gabandé-Rodríguez et al., 2019), estrés oxidativo, metabolismo y autofagia (Bagherniya et al., 2018).
- La restricción calórica también puede prolongar la esperanza de vida al aumentar la expresión de genes que protegen contra el daño y la muerte celular (Komatsu T et al., 2019).
En nuestra evolución normal, nos vimos obligados a restricciones calóricas en nuestro En nuestra evolución normal, nos vimos obligados a restricciones calóricas en nuestro. La respuesta de nuestro cuerpo a la restricción es repararse a sí mismo destruyendo primero las células malas o mutadas o precancerosas para obtener energía y ralentizando el metabolismo. Cuando se ralentiza el metabolismo, se quema menos energía, se reduce el estrés oxidativo y se vive más tiempo. Y la restricción calórica también tiene efectos sobre la expresión genética. Nuestro cuerpo está acostumbrado a ello y lo espera como parte normal de la vida. La falta de autofagia conduce directamente al riesgo de cáncer. A una dieta basada en alimentos vegetales integrales es naturalmente más propensa a inducir una restricción calórica al aportar menos calorías que una dieta americana estándar (DAE) sin dejar de satisfacer las necesidades nutricionales (Greger, 2020). Por otro lado, el TAE provoca un exceso de calorías debido al consumo de aceite y azúcar y de alimentos muy apetecibles, lo que puede perjudicar la expresión genética y aumentar el riesgo de enfermedad.
Efectos de la fibra en la expresión génica.
La fibra es un tipo de hidrato de carbono que no es digerido directamente por nuestras enzimas, sino que va a parar al colon, donde es fermentado por las bacterias intestinales. La fibra puede ayudarte a regular la digestión, reducir el colesterol y prevenir el estreñimiento.
Las bacterias que fermentan la fibra son simbióticas y buenas para nuestro sistema inmunitario y nuestro organismo, a diferencia de las bacterias no probióticas que putrefactan la carne. Esta bacteria carnívora putrefacta la carne que has comido durante horas en el colon causando inflamación. La carne es la carne y la suya también es sabrosa.
Puedes obtener fibra de alimentos como frutas, verduras, cereales, legumbres y frutos secos.
He aquí algunos ejemplos:
- La fibra puede afectar a la composición y función de la microbiota intestinal al proporcionar alimento a las bacterias probióticas y estimular su crecimiento y actividad frente a las bacterias no probióticas que se alimentan de carne (Makki et al., 2018).
- La fibra afecta a los metabolitos producidos por la microbiota intestinal. Los metabolitos son las sustancias que produce o consume la microbiota intestinal. Pueden entrar en el torrente sanguíneo y afectar a los órganos y tejidos. La fibra puede afectar al tipo y la cantidad de estos metabolitos producidos por la microbiota intestinal estimulando las bacterias probióticas y regulando a la baja los procesos metabólicos de las bacterias no probióticas que se alimentan de carne en el colon (Makki et al., 2018).
- Estos metabolitos pueden afectar a la regulación epigenética modulando la disponibilidad o la actividad de donantes químicos o enzimas que controlan la metilación del ADN y las modificaciones de las histonas. Estos cambios epigenéticos pueden alterar la expresión de genes implicados en la inflamación, la inmunidad y el metabolismo.
- La fibra puede proteger contra la obesidad y la diabetes modulando la expresión de genes implicados en la homeostasis de la glucosa, el metabolismo de los lípidos y el gasto energético.
- La fibra puede mejorar la función inmunitaria. La inflamación crónica puede ser consecuencia de un desequilibrio de la microbiota intestinal o de un deterioro de la función de barrera del intestino. La fibra puede mejorar la función inmunitaria y prevenir las infecciones modulando la expresión de genes implicados en la inflamación, la inmunidad y la función de barrera, y reduciendo la actividad y el número de bacterias no probióticas en la colonia de microbiota. La fibra también puede estimular la producción de anticuerpos y citoquinas que ayudan a combatir los gérmenes..
La ingesta dietética recomendada (IDR) de fibra es de 25 gramos al día para las mujeres y de 38 gramos al día para los hombres. Esto es sólo la IDR para la SAD. Desde un punto de vista antropológico, nuestros antepasados homínidos consumían mucho más que eso. Una regla con la fibra es que más suele ser mejor. El problema es que no queremos hinchazón, gases y un aumento constante de las deposiciones. Tampoco nos gusta la textura extraña de la fibra sin sabor, así que preferimos no comerla.
En el siguiente vídeo, el doctor Oded Rechavi, catedrático de neurobiología de la Universidad de Tel Aviv y experto en cómo se heredan los genes, cómo las experiencias moldean los genes y, sorprendentemente, cómo algunos recuerdos de experiencias pueden transmitirse a través de los genes a la descendencia. Habla de sus investigaciones, que ponen en tela de juicio los postulados de la herencia genética, y de la importancia de estos hallazgos para comprender procesos biológicos y psicológicos clave como el metabolismo, el estrés y los traumas. Describe la historia de la exploración científica de la "heredabilidad de los rasgos adquiridos" y cómo la epigenética y la biología del ARN pueden explicar en parte el paso de ciertos recuerdos basados en la experiencia.
Conclusión:
Se trata de un tema muy amplio que está en la primera línea de la investigación científica de las dos últimas décadas. He intentado hacer un resumen en este artículo antes de adentrarnos en algunos escenarios concretos en artículos correlativos.
Estos son sólo algunos ejemplos de cambios epigenéticos y sus efectos sobre el riesgo de cáncer. Hay muchos más factores que pueden provocar cambios epigenéticos, como el tabaquismo, el ejercicio, el estrés, las drogas, la contaminación o los traumatismos.
La conclusión es que tus genes no son fijos. Puedes cambiarlos con tus elecciones y necesitas elegir una dieta rica en antioxidantes, y fibra, evitando la bioacumulación de mutágenos y toxinas en la cadena alimentaria. Necesitas evitar los tipos de dietas hipercalóricas y densas en nutrientes e incorporar la restricción calórica con el ayuno intermitente y evitar sobreexigir tu sistema endocrino con una ingesta excesiva de proteínas. Existe un alto nivel de correlación entre el riesgo general de cáncer y los niveles crónicamente elevados de IGF-1 (debido a una dieta SAD dominada por proteínas de alta calidad).

Así que tome decisiones inteligentes que protejan su expresión genética y reduzcan su riesgo de cáncer. Mi consejo es que no espere cincuenta años más para cambiar las recomendaciones, como hicimos con el tabaco. Usted tiene el poder de cambiar no sólo sus genes, sino también los de sus hijos.
- La genética clásica no podía explicarlo todo, lo que llevó a la creación de la biología molecular.
- La epigenética desafió supuestos y dogmas de la genética y la biología molecular.
- La epigenética expone los mecanismos que regulan la expresión de los genes sin cambiar la secuencia del ADN.
- Lo importante no son los genes, sino la forma en que se expresan.
- Las modificaciones químicas del ADN o las histonas pueden afectar al acceso a los genes y a su utilización.
- Las enzimas pueden añadir o eliminar modificaciones en función de diversos factores.
- Los cambios pueden transmitirse a las células hijas o incluso a los hijos durante la reproducción.
- La epigenética puede influir en rasgos no codificados por el ADN de forma independiente, como el comportamiento, la propensión a enfermedades y el envejecimiento.
- La expresión génica se refiere a la frecuencia o el momento en que se crean proteínas a partir de las instrucciones contenidas en los genes.
- La transcripción puede activarse o desactivarse en función de distintos factores, lo que permite al organismo adaptarse a diferentes situaciones.
- El cáncer implica miles de mutaciones en el genoma y el epigenoma.
- La predisposición genética es sólo un aspecto del cáncer.
- La expresión génica, influida por la dieta y el entorno, puede activar la predisposición genética al cáncer.
- Los cambios epigenéticos pueden afectar al riesgo de desarrollar cáncer y a la respuesta al tratamiento.
- Los cambios epigenéticos pueden afectar al riesgo de desarrollar cáncer y a la respuesta al tratamiento.
- La metilación del ADN bloquea el acceso a los genes, apagándolos y desactivando el sistema inmunitario.
- La metilación puede aumentar el riesgo de cáncer y hacerlo más agresivo.
- La modificación de las histonas puede afectar a genes que regulan el ciclo celular, la apoptosis o la angiogénesis.
- Las mutaciones en varios genes aumentan el riesgo de cáncer, pero la regulación adicional a través de la metilación, la modificación de las histonas o el ARN no codificante puede aumentar aún más el riesgo o dificultar el tratamiento del cáncer.
- Los antioxidantes pueden prevenir o invertir la metilación del ADN causada por radicales libres o toxinas.
- Los antioxidantes pueden modular las modificaciones de las histonas influyendo en las enzimas y cambiando la estructura de la cromatina.
- Los antioxidantes pueden regular el ARN no codificante, alterando la regulación de los genes.
- Los antioxidantes pueden prevenir o reparar daños en el ADN y restablecer la expresión normal de los genes, frenando el desarrollo del cáncer.
- El folato proporciona grupos metilo para la metilación del ADN.
- La carencia de folato puede alterar la metilación del ADN y provocar una expresión génica anormal.
- La carencia de folato puede deteriorar la función cognitiva y aumentar el riesgo de demencia.
- El ácido fólico no es lo mismo que el folato.
- La restricción calórica retrasa el envejecimiento y modula la inflamación, el estrés oxidativo, el metabolismo y las vías de autofagia.
- La restricción calórica aumenta la expresión de genes que protegen contra el daño y la muerte celular.
- La restricción calórica fue una parte normal de nuestra evolución debido a la escasez.
- La restricción calórica fue una parte normal de nuestra evolución debido a la escasez.
- Una dieta integral basada en plantas induce de forma natural la restricción calórica sin dejar de satisfacer las necesidades nutricionales.
- Una dieta integral basada en plantas induce de forma natural la restricción calórica sin dejar de satisfacer las necesidades nutricionales. alimentos muy apetecibles.
- La fibra afecta a la microbiota intestinal estimulando las bacterias probióticas y reduciendo el número de bacterias no probióticas que se alimentan de carne.
- Los metabolitos producidos por la microbiota intestinal pueden afectar a órganos y tejidos, y la fibra puede influir en el tipo y la cantidad de estos metabolitos.
- La fibra puede modular la regulación epigenética y alterar la expresión de genes implicados en la inflamación, la inmunidad y el metabolismo.
- La fibra puede proteger contra la obesidad y la diabetes modulando la expresión de genes implicados en la homeostasis de la glucosa, el metabolismo de los lípidos y el gasto energético.
- La fibra puede mejorar la función inmunitaria modulando la expresión de genes implicados en la inflamación, la inmunidad y la función de barrera, y reduciendo el número de bacterias no probióticas.
- La fibra puede estimular la producción de anticuerpos y citoquinas para combatir los gérmenes.
- Más fibra suele ser mejor.
- Un exceso de fibra puede provocar hinchazón, gases y aumento de las deposiciones.
- Hay muchos factores que pueden provocar cambios epigenéticos, como el tabaco, el ejercicio, el estrés, las drogas, la contaminación o los traumatismos.
- Tus genes no son fijos y pueden cambiar con tus decisiones.
- Se recomienda una dieta rica en antioxidantes y fibra y evitar el bioacumulación de mutágenos y toxinas en una cadena alimentaria.
- Deben evitarse las dietas hipercalóricas y pobres en nutrientes.y se recomienda la restricción calórica con ayuno intermitente.
- Una ingesta excesiva de proteínas puede sobreexpresar el IGF1 y aumentar el riesgo de cáncer.
Preguntas Frecuentes
Referencias:
- Peixoto, P., Cartron, P. F., Serandour, A. A., & Hervouet, E. (2020). De 1957 a nuestros días: A Brief History of Epigenetics. Revista internacional de ciencias moleculares, 21(20), 7571. https://doi.org/10.3390/ijms21207571
- ¿Qué es la epigenética? | CDC. (2022, 15 de agosto). Centros para el Control y la Prevención de Enfermedades. https://www.cdc.gov/genomics/disease/epigenetics.htm
- LaPelusa, A., & Kaushik, R. (2022). Fisiología, Proteínas. En StatPearls. StatPearls Publishing. [PubMed]
- Blackwell, T. K., & Walker, A. K. (2006). Mecanismos de transcripción. WormBook : la revista en línea de biología de C. elegans, 1-16. https://doi.org/10.1895/wormbook.1.121.1
- Hamilton J. P. (2011). Epigenética: principios y práctica. Enfermedades digestivas (Basilea, Suiza), 29(2), 130-135. https://doi.org/10.1159/000323874
- Fanucchi, S., Domínguez-Andrés, J., Joosten, L. A. B., Netea, M. G., & Mhlanga, M. M. (2021). La intersección de la epigenética y el metabolismo en la inmunidad entrenada. Inmunidad, 54(1), 32-43. https://doi.org/10.1016/j.immuni.2020.10.011
- Surace, A. E. A., & Hedrich, C. M. (2019). El papel de la epigenética en las enfermedades autoinmunes/inflamatorias. Fronteras de la inmunología, 10, 1525. https://doi.org/10.3389/fimmu.2019.01525
- Denhardt, D. T. (2018). Efecto del estrés en la biología humana: Epigenética, adaptación, herencia y significado social. Revista de Fisiología Celular, 233(3), 1975-1984. https://doi.org/10.1002/jcp.25837
- de Magalhães-Barbosa, M. C., Prata-Barbosa, A., & da Cunha, A. J. L. A. (2022). Estrés tóxico, epigenética y desarrollo infantil. Revista de pediatría, 98 Suppl 1(Suppl 1), S13-S18. https://doi.org/10.1016/j.jped.2021.09.007
- Cavalli, G., & Heard, E. (2019). Los avances en epigenética vinculan la genética con el medio ambiente y la enfermedad. Naturaleza, 571(7766), 489-499. https://doi.org/10.1038/s41586-019-1411-0
- Brena, R. M., & Costello, J. F. (2007). Interacciones genoma-epigenoma en el cáncer. Genética molecular humana, 16 Especificación nº 1R96-R105. https://doi.org/10.1093/hmg/ddm073
- Shen, H., & Laird, P. W. (2013). Interacción entre el genoma del cáncer y el epigenoma. Celda, 153(1), 38-55. https://doi.org/10.1016/j.cell.2013.03.008
- Hullar, M. A., & Fu, B. C. (2014). Dieta, microbioma intestinal y epigenética. Revista del cáncer (Sudbury, Mass.), 20(3), 170-175. https://doi.org/10.1097/PPO.0000000000000053
- Abdul, Q. A., Yu, B. P., Chung, H. Y., Jung, H. A., & Choi, J. S. (2017). Modificaciones epigenéticas de la expresión génica por el estilo de vida y el entorno. Archivos de investigación farmacológica, 40(11), 1219-1237. https://doi.org/10.1007/s12272-017-0973-3
- Catteau, A., & Morris, J. S. (2002). Metilación de BRCA1: ¿un papel importante en el desarrollo tumoral? Seminarios sobre biología del cáncer, 12(5), 359-371. https://doi.org/10.1016/s1044-579x(02)00056-1
- Prajzendanc, K., Domagała, P., Hybiak, J., Ryś, J., Huzarski, T., Szwiec, M., Tomiczek-Szwiec, J., Redelbach, W., Sejda, A., Gronwald, J., Kluz, T., Wiśniowski, R., Cybulski, C., Łukomska, A., Białkowska, K., Sukiennicki, G., Kulczycka, K., Narod, S. A., Wojdacz, T. K., Lubiński, J., ... Jakubowska, A. (2020). BRCA1 promoter methylation in peripheral blood is associated with the risk of triple-negative breast cancer. Revista internacional del cáncer, 146(5), 1293-1298. https://doi.org/10.1002/ijc.32655
- Yue, X., Zhao, Y., Xu, Y., Zheng, M., Feng, Z., & Hu, W. (2017). Mutant p53 in Cancer: Accumulation, Gain-of-Function, and Therapy. Revista de biología molecular, 429(11), 1595-1606. https://doi.org/10.1016/j.jmb.2017.03.030
- Saliani, M., Jalal, R., & Javadmanesh, A. (2022). Differential expression analysis of genes and long non-coding RNAs associated with KRAS mutation in colorectal cancer cells. Informes científicos, 12(1), 7965. https://doi.org/10.1038/s41598-022-11697-5
- Beetch, M., Harandi-Zadeh, S., Shen, K., Lubecka, K., Kitts, D. D., O'Hagan, H. M., & Stefanska, B. (2020). Dietary antioxidants remodel DNA methylation patterns in chronic disease. Revista británica de farmacología, 177(6), 1382-1408. https://doi.org/10.1111/bph.14888
- Crider, K. S., Yang, T. P., Berry, R. J., & Bailey, L. B. (2012). Folate and DNA methylation: a review of molecular mechanisms and the evidence for folate's role. Avances en nutrición (Bethesda, Md.), 3(1), 21-38. https://doi.org/10.3945/an.111.000992
- Gensous, N., Franceschi, C., Santoro, A., Milazzo, M., Garagnani, P., & Bacalini, M. G. (2019). El impacto de la restricción calórica en las firmas epigenéticas del envejecimiento. Revista internacional de ciencias moleculares, 20(8), 2022. https://doi.org/10.3390/ijms20082022
- Choi, S. W., & Friso, S. (2010). Epigenética: Un nuevo puente entre la nutrición y la salud. Avances en nutrición (Bethesda, Md.), 1(1), 8-16. https://doi.org/10.3945/an.110.1004
- Borzabadi, S., Oryan, S., Eidi, A., Aghadavod, E., Daneshvar Kakhaki, R., Tamtaji, O. R., Taghizadeh, M., & Asemi, Z. (2018). Los efectos de la suplementación con probióticos en la expresión génica relacionada con la inflamación, la insulina y los lípidos en pacientes con enfermedad de Parkinson: Un Ensayo Aleatorizado, Doble Ciego y Controlado con Placebo. Archivos de medicina iraní, 21(7), 289-295. [PubMed]
- Ye, J., Wu, W., Li, Y., & Li, L. (2017). Influencia de la microbiota intestinal en la metilación del ADN y la modificación de las histonas. Enfermedades y ciencias digestivas, 62(5), 1155-1164. https://doi.org/10.1007/s10620-017-4538-6
- Bhattacharjee, S., & Dashwood, R. H. (2020). Epigenetic Regulation of NRF2/KEAP1 by Phytochemicals (Regulación epigenética de NRF2/KEAP1 por fitoquímicos). Antioxidantes (Basilea, Suiza), 9(9), 865. https://doi.org/10.3390/antiox9090865
- Griñán-Ferré, Christian, et al. "Antioxidantes dietéticos, epigenética y envejecimiento cerebral: A Focus on Resveratrol". Oxidative Stress and Dietary Antioxidants in Neurological Diseases, editado por Colin R. Martin y Victor R. Preedy, Academic Press, 2020, pp. 343-57 https://doi.org/10.1016/B978-0-12-817780-8.00022-0
- Chhabria, S. V., Akbarsha, M. A., Li, A. P., Kharkar, P. S., & Desai, K. B. (2015). In situ allicin generation using targeted alliinase delivery for inhibition of MIA PaCa-2 cells via epigenetic changes, oxidative stress and cyclin-dependent kinase inhibitor (CDKI) expression. Apoptosis : revista internacional sobre muerte celular programada, 20(10), 1388-1409. https://doi.org/10.1007/s10495-015-1159-4
- Crider, K. S., Yang, T. P., Berry, R. J., & Bailey, L. B. (2012). Folate and DNA methylation: a review of molecular mechanisms and the evidence for folate's role. Avances en nutrición (Bethesda, Md.), 3(1), 21-38. https://doi.org/10.3945/an.111.000992
- Saitsu, H. (2017). Receptores de folato y cierre del tubo neural. Anomalías congénitas, 57(5), 130-133. https://doi.org/10.1111/cga.12218
- Abraham, K. J., Ostrowski, L. A., & Mekhail, K. (2017). Non-Coding RNA Molecules Connect Calorie Restriction and Lifespan. Revista de biología molecular, 429(21), 3196-3214. https://doi.org/10.1016/j.jmb.2016.08.020
- Patel, S. A., Velingkaar, N., Makwana, K., Chaudhari, A., & Kondratov, R. (2016). La restricción calórica regula la expresión génica del reloj circadiano a través de mecanismos dependientes e independientes de BMAL1. Informes científicos, 6, 25970. https://doi.org/10.1038/srep25970
- Gabandé-Rodríguez, E., Gómez de Las Heras, M. M., & Mittelbrunn, M. (2019). Control de la Inflamación por Miméticos de Restricción Calórica: En la Encrucijada de la Autofagia y la Mitocondria. Células, 9(1), 82. https://doi.org/10.3390/cells9010082
- Bagherniya, M., Butler, A. E., Barreto, G. E., & Sahebkar, A. (2018). El efecto del ayuno o la restricción calórica en la inducción de la autofagia: Una revisión de la literatura. Estudios sobre el envejecimiento, 47, 183-197. https://doi.org/10.1016/j.arr.2018.08.004
- Komatsu, T., Park, S., Hayashi, H., Mori, R., Yamaza, H., & Shimokawa, I. (2019). Mecanismos de la restricción calórica: Una revisión de los genes necesarios para los efectos de prolongación de la vida e inhibición de tumores de la restricción calórica. Nutrientes, 11(12), 3068. https://doi.org/10.3390/nu11123068
- Greger M. (2020). A Whole Food Plant-Based Diet Is Effective for Weight Loss: The Evidence. Revista americana de medicina del estilo de vida, 14(5), 500-510. https://doi.org/10.1177/1559827620912400
- Makki, K., Deehan, E. C., Walter, J., & Bäckhed, F. (2018). El impacto de la fibra dietética en la microbiota intestinal en la salud y la enfermedad del huésped. Célula huésped y microbio, 23(6), 705-715. https://doi.org/10.1016/j.chom.2018.05.012
Contenidos Relacionados
¿Tienes alguna duda acerca de la nutrición y la salud?
Me encantaría saber de usted y responderlas en mi próxima publicación. Agradezco sus aportes y opiniones y espero tener noticias suyas pronto. También te invito a síguenos en Facebook, Instagram y Pinterest para más contenidos sobre dieta, nutrición y salud. Puedes dejar un comentario allí y conectar con otros entusiastas de la salud, compartir tus consejos y experiencias, y recibir apoyo y ánimo de nuestro equipo y nuestra comunidad.
Espero que este post le haya resultado informativo y ameno y que esté preparado para aplicar los conocimientos adquiridos. Si le ha resultado útil, por favor compártelo con tus amigos y familiares que también podrían beneficiarse de ella. Nunca se sabe quién puede necesitar orientación y apoyo en su camino hacia la salud.
– También Te Puede Interesar –

Aprenda Sobre Nutricion
Milos Pokimica es doctor en medicina natural, nutricionista clínico, escritor sobre salud médica y nutrición y asesor en ciencias de la nutrición. Autor de la serie de libros Go Vegan? Revisión de la Ciencia, también dirige el sitio web sobre salud natural GoVeganWay.com.
Descargo De Responsabilidad Médica
GoVeganWay.com le ofrece reseñas de las últimas investigaciones relacionadas con la nutrición y la salud. La información proporcionada representa la opinión personal del autor y no pretende ni implica sustituir el asesoramiento, diagnóstico o tratamiento médico profesional. La información proporcionada tiene fines informativos únicamente y no pretende sustituir la consulta, el diagnóstico y/o el tratamiento médico de un médico o proveedor de atención médica calificado.NUNCA ignore el CONSEJO MÉDICO PROFESIONAL O RETRASAR la BÚSQUEDA de TRATAMIENTO MÉDICO a CAUSA DE ALGO QUE HAYA LEÍDO EN O accesibles a TRAVÉS de GoVeganWay.com
NUNCA APLICAR CUALQUIER cambio de ESTILO de vida O CAMBIOS EN su totalidad COMO UNA CONSECUENCIA DE ALGO QUE HA LEÍDO EN GoVeganWay.com ANTES de CONSULTAR con LICENCIA PROFESIONAL MÉDICO.
En el caso de una emergencia médica, llame a un médico o al 911 inmediatamente. GoVeganWay.com no se recomienda ni aprueba ninguna de los grupos, las organizaciones, las pruebas, los médicos, productos, procedimientos, opiniones u otra información que pueda ser mencionado en el interior.
Selecciones del editor –
Milos Pokimica es escritor especializado en salud y nutrición y asesor en ciencias nutricionales. Autor de la serie de libros Go Vegan? Revisión de la Ciencia, también dirige el sitio web sobre salud natural GoVeganWay.com.
Últimos artículos -
Top Noticias De Salud — ScienceDaily
- Popular GLP-1 weight-loss drugs linked to lower risks of addiction and overdoseen junio 3, 2026
A massive study of more than 600,000 U.S. veterans suggests that popular GLP-1 drugs such as semaglutide may do far more than help with diabetes and weight loss—they could also fight addiction itself. Researchers found that people taking these medications were less likely to develop substance use disorders involving alcohol, nicotine, cannabis, cocaine, opioids, and other drugs, while those already struggling with addiction experienced fewer overdoses, hospitalizations, emergency visits, and […]
- This new diabetes pill burns fat without the downsides of Ozempicen junio 3, 2026
Scientists have developed an experimental diabetes and obesity pill that works in a completely different way from drugs like Ozempic. Rather than reducing hunger, it activates metabolism in skeletal muscle, helping lower blood sugar and increase fat burning while preserving muscle mass. Early clinical results suggest the treatment is safe and well tolerated.
- Scientists reverse anxiety by fixing a tiny brain circuiten junio 3, 2026
A newly identified group of amygdala neurons appears to play a central role in anxiety and social behavior. Restoring normal activity in this tiny brain circuit reversed anxiety and social deficits in mice, revealing a promising new target for future treatments.
- Scientists discovered something surprising about french fries and diabetesen junio 3, 2026
French fries may be the real potato problem. A large study tracking more than 205,000 people for nearly 40 years found that eating three servings of fries per week was linked to a 20% higher risk of developing type 2 diabetes, while baked, boiled, or mashed potatoes showed no significant increase in risk. The research also found that swapping potatoes for whole grains lowered diabetes risk, while replacing them with white rice had the opposite effect.
- Brain scans reveal two distinct types of autismen junio 3, 2026
Scientists have uncovered evidence that autism may include at least two biologically distinct subtypes, each marked by a different pattern of brain communication. By combining brain scans from nearly 1,000 people with autism with insights from 20 genetically engineered mouse models, researchers identified a “hyperconnectivity” subtype, where brain regions communicate more than usual, and a “hypoconnectivity” subtype, where communication is reduced.
- A single protein may be holding back CAR T cancer therapyen junio 2, 2026
A newly identified protein may be one of the biggest obstacles holding CAR T-cell therapy back. Researchers found that NFIL3 causes these engineered immune cells to become exhausted and lose their cancer-fighting power over time. When NFIL3 was disabled, the cells remained stronger for longer and controlled tumors more effectively in animal models.
- Scientists discover gut bacteria that may help protect against autism and ADHDen junio 2, 2026
A major study suggests that some of the groundwork for brain development may be shaped before birth through a surprising partnership between a baby’s genes and gut microbes. Researchers found that epigenetic changes present at birth can influence how the gut microbiome develops during the first year of life, and certain combinations were linked to early signs of autism and ADHD by age three.
PubMed, #Dieta vegana –
- Editorial: Recent insights in vegetarian nutritionen junio 1, 2026
No abstract
- Pet food choices in transition: how owner demographics and diets influence pet food selection and the acceptance of alternative protein sources in pet feedingen junio 1, 2026
Given the increasing interest in alternative protein sources and growing ethical awareness in nutrition, this large-scale survey (n = 8,823) investigated the feeding practices of dog and cat owners in mainly German-speaking countries. The aim was to assess preferences, feeding habits, and the acceptance of novel protein sources such as plant- and insect-based pet foods. The results showed that conventional meat-based diets remained predominant (i.e., 53.05% daily feeding of meat-based dry […]
- Environmental Footprint of a Low-Fat Vegan Diet in People With Type 1 Diabetes: A Secondary Analysis of a Randomized Clinical Trialen mayo 29, 2026
A 12-wk randomized clinical trial found that adults with type 1 diabetes on a low-fat, vegan diet (n = 29) showed greater improvements in insulin sensitivity compared with a portion-controlled diet (n = 29). This secondary analysis calculates the greenhouse gas emissions (GHGEs) and cumulative energy demand (CED) of both diets by linking 3-d dietary records to external data sources. A repeated-measures analysis of variance was performed unadjusted and adjusted for change in energy intake. […]
- Protein intake and preservation of function in old age : Current evidence and present research gapsen mayo 28, 2026
In the past, large observational cohort studies suggested that a higher protein intake might slow the age-associated loss of muscle mass and muscle strength. This observation led to the conclusion that a higher protein intake may contribute to a preservation of function and to the prevention of sarcopenia. Therefore, the German Nutrition Society increased their recommendation for daily protein intake in adults aged ≥ 65 years from 0.8 to 1.0 g/kg body weight (estimated value); however, […]
- Flexitarian dietary patterns and neuropsychiatric multimorbidity among the oldest-old in Chinaen mayo 27, 2026
CONCLUSION: In this nationally representative sample of older Chinese adults, flexitarian dietary patterns were not associated with better neuropsychiatric health and were instead linked to higher odds of depression, cognitive impairment, and their co-occurrence. These results suggest that plant-forward diets in the oldest-old should place greater emphasis on overall dietary quality and nutrient adequacy.
Publicaciones aleatorias –
Publicaciones destacadas -
La última versión desde PubMed, #Dieta basada en plantas –
- Effect of steam-pelleting or extrusion on nutrient digestibility of ground barley or faba bean in growing pigspor U S Ruiz en junio 3, 2026
Plant-based feedstuffs may have limitations in nutrient digestibility and nutritional value for pigs that might be ameliorated using heat processing technologies. Thus, the main objective was to evaluate the effect of steam-pelleting or extrusion on digestibility of starch, crude protein (CP), amino acids (AA), and gross energy (GE) of the two contrasting ingredients barley and faba bean in growing pigs. Barley and faba bean ingredients were ground (2.8-mm hammer mill screen), and a portion […]
- Dose-dependent effects of dietary quercetin supplementation on growth performance, nutrient digestibility, meat composition, bone mineralization, and profitability in broilerspor Md Abu Saied en junio 2, 2026
Objectives: This study aimed to determine the optimal dose of quercetin (plant origin) on growth performance, nutrient digestibility, meat composition, shank mineralization, and production costs in broilers. Materials and Methods: A total of 180 day-old, mixed-sex Ross 308 chicks were randomly assigned to four dietary groups, with five replicates of nine birds per group. The corn-soy-based basal diet provided 2998 kcal metabolizable energy (ME)/kg and 22.94% crude protein (CP) in the starter…
- Quantitative comparison of food-based dietary guidelines: alignment with the Slovenian nutrition guidelines 2025 and Slovenian intakepor Samo Kreft en junio 2, 2026
CONCLUSIONS: The SNG2025 are well aligned with contemporary international and national recommendations and align with widely accepted quantitative ranges for all major food groups. Differences between guidelines reflect cultural framing and quantification rather than conflicting nutritional principles. The SNG2025 demonstrate that contemporary dietary guidelines can integrate quantitative guidance, a plant-forward approach, and sustainability considerations while remaining aligned with…
- Global burden of enteric infectious diseases, diarrhoeal diseases, and corresponding aetiologies, 1990-2023: a systematic analysis for the Global Burden of Disease Study 2023por GBD 2023 Diarrhoeal Disease and Enteric Infectious Diseases Collaborators en junio 2, 2026
BACKGROUND: Enteric infectious diseases claim more than 1 million lives annually and are among the top ten causes of death in children younger than 5 years. Remarkable global investment has been dedicated to enteric infectious disease prevention and control; however, the shifting global health landscape is testing the continuance of progress. To evaluate the current status and guide future interventions, we present the latest epidemiological estimates of enteric infectious diseases from the…
- Plant-Based Eating: Exploring at Home vs Dining Out Behaviours Across Consumer Segmentspor Carla Riverola en junio 2, 2026
A global shift toward predominantly meat-free diets is essential to achieve more sustainable food systems, yet the transition remains far from complete. This paper investigates the systemic and behavioural dynamics shaping the adoption of plant-based eating of veg*ns, meat reducers, and omnivores in different dining settings. We analyse data from 3,014 Australian participants recruited primarily through a plant-based living magazine to uncover the drivers and barriers for choosing plant-based…
- Adherence to the EAT-Lancet diet and neuropsychiatric disorders: a systematic review and meta-analysispor Yuhao Wang en junio 1, 2026
Neuropsychiatric disorders (NPDs) are a leading cause of disability worldwide. The predominantly plant-based EAT-Lancet diet has been proposed to confer neuropsychiatric benefits, yet evidence remains limited. This study synthesized associations between adherence to the EAT-Lancet diet and neuropsychiatric outcomes. We searched PubMed, Web of Science, Embase, Scopus, and ProQuest Dissertations and Theses Global through September 4, 2025. Observational studies reporting associations between…