Expressão dos Genes e Epigenética: Como a Dieta e o Ambiente Moldam a Sua Saúde
Não são os genes que importam, mas a forma como se expressam.
Milos Pokimica
Escrito por: Milos Pokimica
Revisto Clinicamente Por: Dr. Xiùying Wáng, M.D.
Updated Janeiro 5, 2026Principais Conclusões:
-Expressão genética e epigenética são processos dinâmicos e reactivos que regulam a forma como os genes são ligados ou desligados em resposta a vários estímulos.
-Diet e ambiente são dois factores principais que podem influenciar a expressão genética e a epigenética, fornecendo nutrientes, químicos, ou sinais que podem modificar o ADN ou as proteínas que com ele interagem.
- As alterações na expressão dos genes podem ter efeitos significativos na saúde e na prevenção de doenças, alterando as funções celulares, o metabolismo, a inflamação, a imunidade e o envelhecimento do organismo.
Introdução.
A maioria das pessoas está, até certo ponto, familiarizada com a ciência por detrás da genética. Genética ajuda-nos a compreender como funciona a evolução e como herdamos traços dos nossos pais e nos ajuda na medicina, ou antropologia ao compreender como os nossos corpos evoluíram dos hominins para os humanos anatomicamente modernos.
Mas e quanto a epigenética? Está familiarizado com este termo? Sabe que os genes não são estabelecidos em pedra? Sabe como podemos mudar o nosso destino influenciando os nossos genes? É um novo e emergente campo científico da epigenética.
Genética clássica.
Mas como chegámos aqui? Como descobrimos os segredos do ADN e os mecanismos que o regulam?
Tudo começou com um monge chamado Gregor Mendel, que viveu no século XIX. Ele estava curioso sobre como as plantas herdaram traços como a cor da flor e a forma da semente. Ele fez experiências com plantas de ervilha, cruzando-as e contando a descendência. Notou que alguns traços seguiam padrões simples de herança, enquanto outros pareciam misturar-se ou desaparecer. Ele inventou algumas regras que explicavam as suas observações, que agora chamamos leis de herança de Mendel. Ele publicou o seu trabalho em 1865, mas ninguém se importou. Ele morreu sem saber que era o pai do campo mais importante da ciência chamado genética.
Avançar rapidamente para o início do século XX. Alguns cientistas redescobriram o trabalho de Mendel e aperceberam-se de que era genial. Descobriram também que os cromossomas eram feitos de ADN e proteínas e que transportavam as unidades de herança, a que chamavam genes. Descobriram como os genes eram dispostos nos cromossomas, como podiam ser trocados durante a meiose (divisão celular), e como podiam ser mutados por radiação ou químicos. Aprenderam também a mapear genes em cromossomas utilizando análise de ligação e frequências de recombinação. Esta foi a era da genética clássica.
Mas havia um problema. A genética clássica não conseguia explicar tudo. Por exemplo, como é que os genes controlavam os traços? Como é que os genes interagem com o ambiente ou quanto dele tem algum efeito sobre o nosso genoma? Como é que os genes mudaram ao longo do tempo e ao longo das gerações? Estas questões conduziram à criação de uma nova disciplina chamada biologia molecular.
Dogma central.
Em 1953, James Watson e Francis Crick resolveram o estrutura do ADN. Era uma dupla hélice feita de quatro nucleótidos (A, T, C, G) que se pareciam um com o outro de uma forma específica (A com T, C com G). Perceberam que esta estrutura explicava como o ADN podia armazenar informação (a sequência de nucleótidos), copiar-se a si próprio (separando os fios e utilizando-os como modelos), e expressar-se (sendo transcrito em ARN e traduzido em proteínas). Este trabalho tornou-se o "dogma central da biologia molecular". Uma teoria afirma que a informação genética flui apenas numa direcção, do ADN, ao ARN, às proteínas, ou o ARN directamente às proteínas. Foi declarado pela primeira vez por Francis Crick em 1957 e publicado em 1958.
Mas havia outro problema. A biologia molecular também não conseguia explicar tudo.
Por exemplo, como é que as células sabiam quando e onde ligar e desligar os genes? Durante o desenvolvimento, como é que as células se dividiram em tipos distintos porque cada uma delas tem o mesmo ADN? Como é que as células se lembraram da sua identidade e história, que é importante para a investigação do cancro? Como é que as células reagiram aos sinais de outras células ou do ambiente?
Nascimento da epigenética.
Estas questões conduziram ao nascimento da epigenética, que visava revelar os mecanismos que regulam a expressão genética sem alterar a sequência de ADN.
O termo epigenética foi cunhado por Conrad Waddington em 1942, mas levou décadas para obter aceitação científica.
A epigenética é baseada na ideia de que existem modificações químicas no ADN ou em histones (proteínas que envolvem o ADN) que podem afectar a forma como os genes são acedidos e utilizados pela maquinaria celular. Estas modificações podem ser adicionadas ou removidas por enzimas, dependendo de vários factores, tais como o tipo de célula, a fase de desenvolvimento, sinais ambientais, stress, dieta, etc. (Peixoto et al., 2020). Estas alterações podem também ser transmitidas às células filhas durante a divisão celular, ou mesmo aos filhos durante a reprodução.
Isto significa que a epigenética pode influenciar traços que não são codificados apenas pelo ADN, tais como comportamento, susceptibilidade a doenças, ou envelhecimento.
A epigenética é um dos temas mais quentes como o genético foi ainda mais uma vez. O problema é que a maioria das pessoas não ouviu falar disso, pelo que a velha crença continua a ser que os genes são tudo. Precisamos de popularizar a nova investigação junto do público em geral, que ainda acredita que os genes estão gravados na pedra e que não há nada que se possa fazer a esse respeito. A epigenética desafia alguns dos pressupostos e dogmas da genética e da biologia molecular. Abre novas possibilidades para compreender a vida a um nível mais profundo. Abre também novas vias para melhorar a medicina e a saúde, modificando a expressão genética.
Não são os genes que importam, mas a forma como se expressam.
O que é a Expressão Genética?
Antes de nos debruçarmos mais cientificamente sobre a epigenética, falemos da expressão genética.
A expressão genética refere-se à frequência ou ao momento em que as proteínas são criadas a partir das instruções contidas nos genes (What Is Epigenetics? | CDC, 2022b).
As proteínas são os blocos de construção. Desempenham muitas funções, como a construção de tecidos, o combate a infecções e a regulação de hormonas (Pelusa et al., 2022).
Os seus genes transportam a informação para produzir proteínas, mas eles próprios não produzem proteínas. Requerem a assistência de outras moléculas, como ARN e enzimas, para ler o código e produzir as proteínas. Este processo é designado por transcrição (Blackwell et al., 2006).
A transcrição nem sempre é feita. Pode estar ligada ou desligada dependendo de diferentes factores, tais como sinais de outras células, hormonas, ou nutrientes. É assim que o nosso corpo se adapta a diferentes situações.
Por exemplo, quando se tem fome, o corpo activa genes que fazem com que as enzimas decomponham os alimentos e libertem energia. Quando está cheio, o seu corpo desliga esses genes e liga genes que armazenam o excesso de energia como gordura.
Porque é que a epigenética é importante?
Epi significa acima ou "no topo de" em grego. Não são os genes que importam, mas o que eles expressam.
Todas as suas células têm os mesmos genes, mas têm um aspecto e um comportamento diferentes devido a alterações epigenéticas. Por outras palavras, é uma camada adicional de informação que controla a regulação dos genes (Hamilton et al., 2011).
As modificações epigenéticas podem inibir ou ativar a expressão dos genes. Uma combinação destas modificações desempenha um papel importante no “imprinting”, um tipo de “marca” que determina se um gene será expresso ou não.
O ADN é formado por combinações de nucleótidos. Estas são as famosas letras que a maioria das pessoas conhece, adenina (A), tiamina (T), guanina (G), e citosina (C).
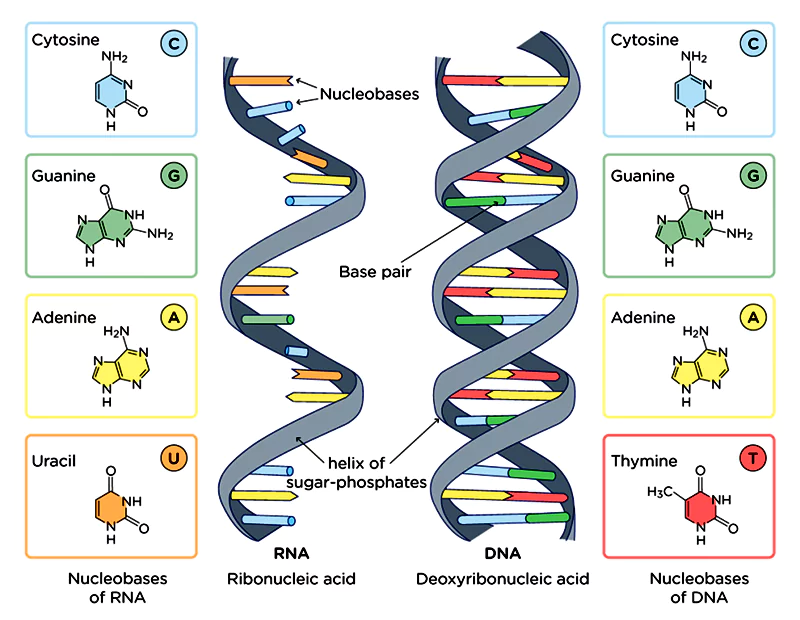
A citosina, por exemplo, pode ser alterada através da adição de um grupo metilo (CH3).
Este processo é conhecido como metilação, e altera a expressão do gene cuja sequência foi alterada. A metilação do ADN conduz tipicamente ao silenciamento do gene. Nas circunstâncias erradas, isto pode ser muito mau se o gene regular a função imunitária ou alguma outra função importante.
As mudanças epigenéticas podem acontecer mesmo antes de nascer, durante o seu desenvolvimento, e ao longo da sua vida. Algumas mudanças epigenéticas são normais e necessárias para o seu crescimento e função.
Outras mudanças epigenéticas são influenciadas pelos seus comportamentos e ambiente.
Por exemplo, o que se come pode afectar a forma como os seus genes são metilados ou como as suas histórias são modificadas.
A sua actividade física pode afectar a quantidade de RNA não codificado produzido ou a forma como interage com a codificação do RNA.
Estas mudanças epigenéticas fazem parte da evolução e têm o seu objectivo, mas também em alguns cenários podem ter efeitos positivos ou negativos na sua saúde.
Algumas alterações epigenéticas, por exemplo, podem melhorar o nosso sistema imunitário activando genes que combatem inflamações ou cancro.
Outras alterações epigenéticas podem aumentar o risco de doenças ao desactivar genes que regulam o metabolismo ou o sistema imunitário (Fanucchi et al, 2021); (Surace et al., 2019).
Isto é uma força motriz de adaptação e evolução. Se quer uma prova de evolução e como funciona em tempo real e como os organismos evoluem, é isto. Esta é uma razão pela qual as mudanças epigenéticas também podem ser herdadas de uma geração para outra. Por exemplo, se os seus avós foram expostos a toxinas, mutagénicos ou factores de stress e se essa exposição resultou em alterações epigenéticas no seu ADN ou nos seus espermatozóides ou óvulos, essas alterações podem ser transmitidas a si e afectar a sua expressão genética (Denhardt et al., 2018).
Ter um ambiente poluído e toxinas por todo o lado não afectará apenas o seu ADN, mas também o ADN dos seus filhos (de Magalhães-Barbosa et al., 2022).
Mudanças epigenéticas e seus efeitos na saúde.
O quadro abaixo ilustra os principais factores que influenciam a expressão genética e as alterações epigenéticas. Há mais factores mas o que se pode retirar desta tabela é o facto de em cada fila os factores que influenciam o risco serem a dieta, o stress e a exposição a toxinas.
| Mudanças epigenéticas | Efeitos na saúde | Fontes |
| Metilação de ADN | Um processo que adiciona grupos metilo às bases do ADN, afectando a expressão genética. Variáveis ambientais como a alimentação, o stress e a exposição tóxica podem todos alterar a metilação do ADN. A metilação do ADN pode afectar vários aspectos da saúde, tais como o risco de cancro, a função imunitária e o envelhecimento. | Cavalli et al., 2019 |
| Modificações do Histone | Um processo que altera a estrutura dos histones, as proteínas que envolvem o ADN. As modificações do histone podem afectar o quão apertado ou frouxo o ADN é embalado, afectando a expressão genética. As modificações do histone podem ser influenciadas por factores ambientais tais como dieta, stress, e exposição a toxinas. As modificações de histone podem afectar vários aspectos da saúde, tais como o risco de cancro, função imunológica e envelhecimento. | Cavalli et al., 2019 |
| RNA não codificador | RNA que não codifica para proteínas. Factores ambientais como dieta, stress, e exposição a toxinas podem todos afectar o RNA não codificador. O ARN não codificador pode ter um impacto em muitas áreas da saúde, incluindo risco de cancro, função imunológica, e envelhecimento. | Cavalli et al., 2019 |
| Infecções | Os germes podem alterar a sua epigenética para enfraquecer o seu sistema imunitário. Isto ajuda o germe a sobreviver. Exemplo: Mycobacterium tuberculosis causa a tuberculose. A tuberculose era e ainda pode ser uma doença fatal porque pode alterar a metilação do ADN das células imunitárias, tornando assim o sistema imunitário menos eficaz no combate à infecção. | What Is Epigenetics? | CDC, 2022b |
Exemplos de alterações epigenéticas e os seus efeitos sobre o risco de cancro.
O cancro é uma doença complexa que envolve milhares de mutações diferentes que se acumulam e envolvem alterações no genoma e no epigenoma (Brena et al., 2007), (Shen et al., 2013). Podemos ter uma predisposição genética para sermos desanimados por causa dos nossos pais, mas isso é apenas uma parte de todo o quadro.
Essa predisposição genética para o cancro liga-se, de facto, em função da expressão genética e a expressão genética depende sobretudo de uma dieta (Hullar et al., 2014), e ambiente (Abdul et al., 2017).
As alterações epigenéticas podem ligar ou desligar genes que estão envolvidos no crescimento celular, morte celular, ou resposta imunológica. Estas alterações podem então afectar o seu risco global de desenvolver cancro ou de responder ao tratamento do cancro. É por isso que temos uma epidemia de cancro em que uma em cada quatro pessoas nas sociedades ocidentais com uma dieta padrão americana, morrerá dela. Não são os maus genes que são uma causa, mas a expressão genética.
Eis alguns exemplos de alterações epigenéticas e dos seus efeitos sobre o risco de cancro:
- A metilação do ADN impede que as proteínas que lêem o gene acedam ao mesmo, essencialmente desligando o gene. A metilação do ADN pode desligar genes que suprimem tumores ou reparam danos no ADN, basicamente desactivando o sistema imunitário. Por exemplo, ter uma mutação no gene BRCA1 que o impede de funcionar correctamente aumenta a probabilidade de contrair cancro da mama e alguns outros tipos de cancro. No entanto, se este gene também estiver metilado, o mais provável é morrer porque o seu sistema imunitário está desligado. A metilação pode aumentar ainda mais o risco de cancro e torná-lo mais agressivo (Catteau et al., 2002), (Prajzendanc et al., 2020).
- A modificação do histone é quando grupos químicos são adicionados ou removidos dos histones, que são proteínas que se envolvem em torno do ADN para formar uma estrutura chamada cromatina. Dependendo do tipo e localização dos grupos químicos, a modificação de histone pode tornar a cromatina mais apertada ou frouxamente embalada, afectando a quantidade de ADN exposto ou escondido das proteínas que a lêem. A modificação do histone pode afectar os genes que regulam o ciclo celular, Por exemplo, ter uma mutação no gene p53 que o impede de funcionar correctamente torna mais provável a obtenção de vários cancros. Contudo, se este gene também for modificado por histones, pode aumentar ainda mais o risco de cancro ou tornar o seu cancro mais resistente ao tratamento (Yue et al., 2017).
- RNA não codificado: Isto é quando moléculas chamadas RNA não codificante são anexadas ao RNA codificante, que é usado para fazer proteínas. O RNA não codificante pode ajudar a quebrar o RNA codificante ou recrutar moléculas que modificam histórias, afectando a expressão genética. O RNA não codificante pode afectar genes que controlam a diferenciação celular, invasão, ou metástase. Por exemplo, ter uma mutação no gene KRAS que o impede de funcionar correctamente torna-o mais susceptível de contrair cancro colorrectal. No entanto, se este gene também for regulado por RNA não codificante, pode aumentar ainda mais o risco de cancro ou tornar o seu cancro mais difícil de tratar (Saliani et al., 2022).
Mudanças epigenéticas e seus efeitos em função da dieta e da nutrição
| Componentes dietéticos | Mudanças epigenéticas | Fontes |
| Antioxidantes | Os antioxidantes são moléculas que podem neutralizar os radicais livreso que pode danificar o ADN e as histórias. Os antioxidantes podem modular as alterações epigenéticas, afectando a metilação do ADN e as modificações do histone. | Beetch et al., 2020 |
| Folato | O folato é uma vitamina B que está envolvida na síntese de ADN e ARN. O folato pode afectar as alterações epigenéticas ao fornecer grupos metilo para a metilação do ADN. A deficiência de folato pode prejudicar a metilação do ADN e aumentar o risco de várias doenças, tais como o cancro, defeitos do tubo neural e deficiência cognitiva. | Crider et al., 2012 |
| Restrição calórica | A restrição calórica é uma intervenção dietética que reduz a ingestão de calorias sem causar desnutrição pela desregulamentação de vários factores, tais como inflamação, stress oxidativo, e taxa metabólica basal. A restrição de calorias pode afectar as alterações epigenéticas ao alterar a expressão e actividade das enzimas envolvidas na metilação do ADN e nas modificações do histoneto. | Gensous et al., 2019 |
| Fibra | A fibra é um tipo de carboidrato que não é digerido por enzimas humanas, mas que pode ser fermentado por bactérias intestinais. A fibra pode afectar as alterações epigenéticas influenciando a composição e função da microbiota intestinal, que pode produzir metabolitos que modulam a metilação do ADN e as modificações do histoneto. | Choi et al., 2010 |
| Probióticos | Os probióticos podem afectar as alterações epigenéticas influenciando a composição e função da microbiota intestinal, que pode produzir metabolitos que modulam a metilação do ADN e as modificações do histoneto. Os probióticos também podem modular a expressão dos genes envolvidos na inflamação, imunidade e metabolismo. | (Borzabadi et al., 2018), (Ye et al., 2017) |
| Prebióticos | Os prebióticos são hidratos de carbono não digeríveis que estimulam selectivamente o crescimento e/ou actividade de bactérias intestinais benéficas. Os prebióticos podem afectar as alterações epigenéticas influenciando a composição e função da microbiota intestinal, que pode produzir metabolitos que modulam a metilação do ADN e as modificações do histone. Os prebióticos também podem modular a expressão dos genes envolvidos na inflamação, imunidade e metabolismo. | Ye et al., 2017 |
Efeito dos antioxidantes na expressão dos genes.
Aqui estão alguns exemplos que não é uma lista completa de todos os efeitos, apenas um exemplo:
- Os antioxidantes podem prevenir ou reverter a metilação do ADN. A metilação do ADN pode acontecer quando se é exposto a radicais livres ou toxinas. Os antioxidantes podem bloquear este processo ou remover o grupo metilo, restaurando a função do gene.
- Os antioxidantes podem modular as modificações do historial. Os antioxidantes podem influenciar as enzimas que fazem estas modificações, alterando a estrutura da cromatina.
- Os antioxidantes podem regular o RNA não codificador. Os antioxidantes podem afectar a produção ou actividade do RNA não codificante, alterando a regulação genética.
- Os antioxidantes podem prevenir ou reparar danos no ADN e restaurar a expressão normal dos genes, prevenindo ou retardando o desenvolvimento do cancro.
No quadro abaixo estão seleccionados antioxidantes e os seus efeitos na expressão genética. Esta não é uma lista completa, apenas alguns exemplos que foram pesquisados pelo cientista. Existem milhares de fitoquímicos diferentes e deverá ou não ser capaz de os investigar a todos. Deve esforçar-se por aumentar a valor global ORAC da sua dieta através da nutrição e não seguir a via dos antioxidantes individuais suplementares. Os fitoquímicos funcionam sinergicamente como um complexo de produtos químicos de fontes alimentares inteiras onde 2 mais 2 é igual a 15. Na tabela, enumerei alguns antioxidantes apenas a título de exemplo.
| Antioxidante | Efeito na epigenética | Fonte |
| Curcumina | A curcumina é um polifenol anti-inflamatório, antioxidante, e anticancerígeno produzido a partir de curcuma. A curcumina pode inibir as metiltransferases de DNA (DNMTs) e as deactilases histónicas (HDACs), provocando a reactivação dos genes supressores do tumor e a supressão de oncogenes. A curcumina também pode alterar a estrutura da cromatina e a expressão dos genes induzindo a acetilação e a metilação do histone. A curcumina pode modular microRNAs (miRNAs) e RNAs longos não codificantes (lncRNAs), ambos genes alvo envolvidos em inflamação, apoptose, ciclo celular, invasão, e metástase. | Bhattacharjee et al., 2020 |
| Resveratrol | Resveratrol é um polifenol natural encontrado em uvas, vinho tinto, bagas e amendoins que tem efeitos antioxidantes, anti-inflamatórios, e anticancerígenos. O Resveratrol pode inibir DNMTs e HDACs, resultando na desmetilação e reactivação de genes supressores de tumores e na desregulação de oncogenes. O resveratrol pode também induzir a acetilação e a metilação do histone, afectando a estrutura da cromatina e a expressão dos genes. O resveratrol pode regular miRNAs e lncRNAs que visam genes envolvidos em stress oxidativo, inflamação, apoptose, autofagia, senescência, angiogénese, e metástase. | Griñán-Ferré et al., 2020 |
| Apigenina | A apigenina é um flavonóide natural derivado de flores de camomila, laranjas, salsa, aipo, e outras fontes naturais que tem propriedades antioxidantes, anti-inflamatórias, e anticancerígenas. A apigenina pode inibir DNMTs e HDACs, levando à desmetilação e reactivação dos genes supressores de tumores e à desregulação dos oncogenes. A apigenina pode também induzir a acetilação e a metilação do histone, alterando a estrutura da cromatina e a expressão dos genes. A apigenina pode regular os miRNAs que visam genes envolvidos no ciclo celular, apoptose, invasão, metástase, angiogénese, e estaminais. | Bhattacharjee et al., 2020 |
| Sulforafano | O sulforafano é um isotiocianato natural derivado de vegetais cruciferos, tais como os brócolos, couve, e couve que tem propriedades antioxidantes, anti-inflamatórias, e anticancerígenas. O sulforafano pode inibir DNMTs e HDACs, levando à desmetilação e reactivação dos genes supressores de tumores e à desregulação de oncogenes. O sulforafano também pode induzir a acetilação e a metilação do histone, alterando a estrutura da cromatina e a expressão dos genes. O sulforafano pode regular miRNAs e lncRNAs que visam genes envolvidos em inflamação, apoptose, ciclo celular, invasão, e metástase. | Bhattacharjee et al., 2020 |
| Ácido ursólico | O ácido ursólico é um triterpenoide pentacíclico natural encontrado em várias frutas, ervas e especiarias que tem efeitos antioxidantes, anti-inflamatórios, e anticancerígenos. O ácido ursólico pode inibir DNMTs e HDACs, resultando na desmetilação e reactivação de genes supressores de tumores e na desregulação de oncogenes. O ácido ursólico pode também induzir a acetilação e a metilação do histone, afectando a estrutura da cromatina e a expressão dos genes. O ácido ursólico pode regular os miRNAs que visam os genes envolvidos no ciclo celular, apoptose, invasão, metástase, angiogénese, e estaminais. | Bhattacharjee et al., 2020 |
| Allicina | A alicina é um composto natural de enxofre derivado de alho que tem efeitos antimicrobianos, antioxidantes, anti-inflamatórios, e anticancerígenos. A alicina pode inibir a actividade da giramase do ADN em bactérias, levando à inibição da replicação e transcrição do ADN. A alicina também pode oxidar resíduos de cisteína em proteínas, afectando a sua estrutura e função. A alicina pode regular os miRNAs que visam genes envolvidos no ciclo celular, apoptose, invasão, metástase, angiogénese, e estaminais. | Chhabria et al., 2015 |
Há muito mais antioxidantes que podem afectar a expressão genética. Se quiser saber mais, pode procurar artigos correlacionados.
Pode também estar a perguntar-se de onde pode obter antioxidantes. A boa notícia é que se encontram sobretudo em plantas e que há plantas muito ricas em conteúdo antioxidante. Aprenda os seus valores ORAC.
Efeitos do folato na expressão genética.
O folato é uma vitamina B que está envolvida na síntese de ADN e ARN. Precisa de folato para que as suas células cresçam e se dividam adequadamente. Pode obter folato a partir de alimentos como folhas verdes, feijões, nozes, ovos, e cereais fortificados. O problema é que este é um dos mais predominantes deficiências na dieta padrão americana. As pessoas que comem uma dieta à base de plantas integrais não são normalmente deficientes em folato e não necessitam de um suplemento adicional de ácido fólico.
Aqui estão alguns exemplos:
- O folato fornece grupos metilo (um grupo de carbono) para a metilação do ADN (Crider et al., 2012). O folato é uma das principais fontes de grupos metilo para este processo. A deficiência de folato pode prejudicar a metilação do ADN e causar uma expressão genética anormal.
- O folato afecta o encerramento do tubo neural. O tubo neural é a estrutura que forma o cérebro e a medula espinal no embrião. O tubo neural precisa de se fechar correctamente para um desenvolvimento normal. O folato é essencial para este processo porque afecta a expressão dos genes envolvidos no encerramento do tubo neural (Saitsu et al., 2017). A deficiência de folato pode impedir o fecho do tubo neural e causar defeitos congénitos como a espinha bífida.
- O folato é importante para a função cognitiva porque afecta a expressão dos genes envolvidos no desenvolvimento e função cerebral. A deficiência de folato pode prejudicar a função cognitiva e aumentar o risco de demência.
Estes são alguns dos efeitos do folato sobre a epigenética e porque são importantes para a sua saúde e desenvolvimento. Pode estar a perguntar-se de quanto folato precisa e de onde o pode obter. Bem, aqui estão algumas dicas:
- O RDA para folato é de 400 microgramas para adultos e 600 mcg para mulheres grávidas.
- Pode-se obter folato de alimentos como verduras de folhas, feijões, nozes, ovos, e cereais fortificados. Também pode tomar um suplemento se tiver uma deficiência ou uma maior necessidade de folato.
- Deve-se evitar tomar demasiado folato porque pode mascarar uma vitamina deficiência de B12 ou interferir com alguns medicamentos.
- Também o ácido fólico não é o mesmo que o folato. Precisamos de folato, mas os suplementos são feitos de ácido fólico. O nosso fígado ao contrário do fígado de ratos no modelo animal é incapaz de converter mais de 400mg de ácido fólico em folato num dia. É por isso que a maioria dos suplementos nunca excedem mais de 400mg de ácido fólico.
Efeitos de restrição calórica na expressão genética.
A restrição calórica é quando se reduz a ingestão de calorias sem causar desnutrição. A restrição calórica pode afectar a quantidade de ARN não codificante produzido ou a forma como este interage com o ARN codificante (Abraham et all., 2017). A restrição calórica pode também regular o ritmo circadiano da expressão genética em diferentes órgãos e tecidos (Patel et al., 2016).
Estes efeitos de restrição calórica na epigenética podem ter vários benefícios para a sua saúde e envelhecimento. Por exemplo:
- A restrição calórica pode retardar o envelhecimento através da modulação de várias vias, como a inflamação (Gabandé-Rodríguez et al., 2019), stress oxidativo, metabolismo e autofagia (Bagherniya et al., 2018).
- A restrição calórica pode também prolongar o tempo de vida, aumentando a expressão de genes que protegem contra os danos e a morte celular (Komatsu T et al., 2019).
Na nossa evolução normal, fomos forçados a restrições calóricas no nosso ambiente normal para todos os nossos antepassados hominídeos devido à escassez. A resposta do nosso corpo à restrição é reparar-se a si próprio, destruindo primeiro as células más, mutantes ou pré-cancerosas para obter energia e abrandando o metabolismo. Quando abrandamos o metabolismo, queimamos menos energia, temos menos stress oxidativo e vivemos mais tempo. E a restrição calórica também tem efeitos na expressão dos genes. O nosso corpo está habituado a ter autofagia e espera que seja uma parte normal da vida. A falta de autofagia conduz diretamente ao risco de cancro. A a dieta baseada em plantas integrais está naturalmente mais inclinada a induzir a restrição calórica fornecendo menos calorias do que uma Dieta Americana Padrão (SAD) e, ao mesmo tempo, satisfazendo as necessidades nutricionais (Greger, 2020). Por outro lado, o SAD provoca um excesso de calorias devido ao óleo e ao açúcar e a alimentos altamente palatáveis, o que pode afectar a expressão genética e aumentar o risco de doença.
Efeitos das fibras na expressão genética.
A fibra é um tipo de carboidrato que não é directamente digerido pelas nossas enzimas, mas acaba no cólon onde é fermentado por bactérias intestinais. A fibra pode ajudar a regular a digestão, baixar o colesterol, e prevenir a obstipação.
As bactérias que fermentam a fibra são simbióticas e boas para o nosso sistema imunitário e corpo, ao contrário das bactérias não bióticas que apodrecem a carne. Esta bactéria que come carne putrefaz a carne que comeu durante horas no cólon, causando inflamação. A carne é carne e a sua também é saborosa.
Pode-se obter fibras de alimentos como frutas, vegetais, grãos, feijões e nozes.
Aqui estão alguns exemplos:
- As fibras podem afectar a composição e a função do microbiota intestinal, fornecendo alimentos às bactérias probióticas e estimulando o seu crescimento e actividade contra as bactérias não probióticas que comem carne (Makki et al., 2018).
- As fibras afectam os metabolitos produzidos pelo microbiota intestinal. Os metabolitos são as substâncias que são produzidas ou consumidas pelo microbiota intestinal. Podem entrar na corrente sanguínea e afectar os órgãos e os tecidos. A fibra pode afectar o tipo e a quantidade destes metabolitos produzidos pelo microbiota intestinal, estimulando as bactérias probióticas e desregulando os processos metabólicos das bactérias não probióticas comedoras de carne no cólon (Makki et al., 2018).
- Estes metabolitos podem então afectar a regulação epigenética, modulando a disponibilidade ou actividade de dadores químicos ou enzimas que controlam a metilação do ADN e as modificações do historial. Estas alterações epigenéticas podem alterar a expressão dos genes envolvidos na inflamação, imunidade, e metabolismo.
- As fibras podem proteger contra a obesidade e a diabetes, modulando a expressão dos genes envolvidos na homeostase da glicose, metabolismo lipídico e gasto energético.
- A fibra pode melhorar a função imunitária. A inflamação crónica pode ser uma consequência de um desequilíbrio da microbiota intestinal ou da função da barreira intestinal deficiente. A fibra pode melhorar a função imunitária e prevenir infecções através da modulação da expressão de genes envolvidos na inflamação, imunidade e função de barreira e através da regulação negativa da atividade e do número de bactérias não probióticas na colónia de microbiota. As fibras podem também estimular a produção de anticorpos e citocinas que ajudam a combater os germes.
A ingestão dietética recomendada (IDR) de fibra é de 25 gramas por dia para as mulheres e 38 gramas por dia para os homens. Isto é apenas RDA para SAD. Num sentido antropológico, os nossos antepassados da hominina consumiram muito mais do que isso. Uma regra com fibra é que mais é normalmente melhor. O problema é que não queremos inchaço, gás, e movimentos intestinais constantemente aumentados. Também não gostamos da textura funky da fibra, sem sabor, por isso preferimos não a comer.
No vídeo abaixo Oded Rechavi, Ph.D., professor de neurobiologia na Universidade de Tel Aviv e especialista em como os genes são herdados, como as experiências moldam os genes, e notavelmente, como algumas memórias de experiências podem ser transmitidas através dos genes aos descendentes. Ele discute a sua investigação desafiando princípios há muito defendidos da herança genética e a relevância dessas descobertas para a compreensão de processos biológicos e psicológicos chave, incluindo metabolismo, stress e trauma. O autor descreve a história da exploração científica da "hereditariedade dos traços adquiridos" e a forma como a epigenética e a biologia do ARN podem explicar parte da passagem de certas memórias baseadas na experiência.
Conclusão:
Este é um vasto tópico que está na linha da frente da investigação científica nas últimas duas décadas. Tentei fazer um resumo neste artigo antes de entrarmos em alguns cenários específicos em artigos correlacionados.
Estes são apenas alguns exemplos de alterações epigenéticas e dos seus efeitos sobre o risco de cancro. Muitos mais factores podem causar alterações epigenéticas, tais como fumar, exercício, stress, drogas, poluição, ou traumas.
O resultado final é que os seus genes não são fixos. Pode mudá-los com as suas escolhas e precisa de escolher uma dieta rica em antioxidantes, e fibras, evitando a bioacumulação de mutagéneos e toxinas numa cadeia alimentar. É necessário evitar tipos de dieta demasiado calórica e densa, com privação de nutrientes e incorporar restrições calóricas com jejum intermitente, e evitar a sobreexpressão do seu sistema endócrino com ingestão excessiva de proteínas. Existe um elevado nível de correlação entre o risco global de cancro e níveis cronicamente elevados de IGF-1 (devido a uma dieta SAD dominada por proteínas de alta qualidade).

Portanto, faça escolhas inteligentes que protejam a sua expressão genética e reduzam o seu risco de cancro. O meu conselho é que não espere mais cinquenta anos antes que as recomendações mudem, como fizemos com o tabaco. Tem o poder de mudar não só os seus genes, mas também os genes dos seus filhos.
- A genética clássica não podia explicar tudo, levando à criação da biologia molecular.
- A epigenética desafiou pressupostos e dogmas da genética e da biologia molecular.
- A epigenética expõe mecanismos que regulam a expressão genética sem alterar a sequência de ADN.
- Não são os genes que importam, mas a forma como se expressam.
- As modificações químicas no ADN ou histonas podem afectar a forma como os genes são acedidos e utilizados.
- As modificações podem ser adicionadas ou removidas por enzimas com base em vários factores.
- As alterações podem ser transmitidas às células filhas ou mesmo às crianças durante a reprodução.
- A epigenética pode influenciar traços não codificados pelo ADN independentemente, tais como comportamento, susceptibilidade a doenças, e envelhecimento.
- A expressão génica refere-se à frequência ou quando as proteínas são criadas a partir das instruções dentro dos genes.
- A transcrição pode estar ligada ou desligada dependendo de diferentes factores, permitindo que o corpo se adapte a diferentes situações.
- O cancro envolve milhares de mutações no genoma e no epigenoma.
- A predisposição genética é apenas um aspecto do cancro.
- A expressão dos genes, influenciada pela dieta e pelo ambiente, pode activar a predisposição genética para o cancro.
- As alterações epigenéticas podem afectar o risco de desenvolvimento de cancro e a resposta ao tratamento.
- A elevada incidência de cancro nas sociedades ocidentais com uma dieta padrão americana deve-se à expressão genética e não a genes maus.
- A metilação do ADN bloqueia o acesso aos genes, desligando os genes e desactivando o sistema imunitário.
- A metilação pode aumentar o risco de cancro e tornar o cancro mais agressivo.
- A modificação do histone pode afectar genes que regulam o ciclo celular, apoptose, ou angiogénese.
- As mutações em vários genes aumentam o risco de cancro, mas uma regulação adicional através da metilação, modificação do histone, ou RNA não codificante pode aumentar ainda mais o risco ou tornar o cancro mais difícil de tratar.
- Os antioxidantes podem prevenir ou reverter a metilação do ADN causada por radicais livres ou toxinas.
- Os antioxidantes podem modular as modificações da história influenciando as enzimas e alterando a estrutura da cromatina.
- Os antioxidantes podem regular o RNA não codificante, alterando a regulação genética.
- Os antioxidantes podem prevenir ou reparar danos no DNA e restaurar a expressão normal dos genes, retardando o desenvolvimento do cancro.
- O folato fornece grupos metilo para a metilação do ADN.
- A deficiência de folato pode prejudicar a metilação do ADN e causar uma expressão genética anormal.
- A deficiência de folato pode prejudicar a função cognitiva e aumentar o risco de demência.
- O ácido fólico não é o mesmo que o folato.
- A restrição calórica abranda o envelhecimento e modula a inflamação, o stress oxidativo, o metabolismo e as vias de autofagia.
- A restrição calórica aumenta a expressão de genes que protegem contra os danos celulares e a morte.
- A restrição calórica foi uma parte normal da nossa evolução devido à escassez.
- O nosso corpo responde à restrição reparando-se a si próprio e retardando o metabolismo.
- Uma dieta alimentar integral à base de plantas induz naturalmente a restrição calórica enquanto ainda satisfaz as necessidades nutricionais.
- A dieta padrão americana (SAD) leva ao excesso calórico e ao aumento do risco de doenças devido ao petróleo, açúcar, e alimentos altamente palatáveis.
- A fibra afecta a microbiota intestinal estimulando as bactérias probióticas e diminuindo o número de bactérias comedoras de carne não-bióticas.
- Os metabolitos produzidos pela microbiota intestinal podem afectar órgãos e tecidos e as fibras podem afectar o tipo e quantidade destes metabolitos.
- A fibra pode modular a regulação epigenética e alterar a expressão genética envolvida na inflamação, imunidade, e metabolismo.
- As fibras podem proteger contra a obesidade e diabetes através da modulação da expressão genética envolvida na homeostase da glucose, metabolismo lipídico, e gasto de energia.
- A fibra pode melhorar a função imunológica ao modular a expressão genética envolvida na inflamação, imunidade e função de barreira e ao diminuir o número de bactérias não bióticas.
- A fibra pode estimular a produção de anticorpos e citocinas para combater os germes.
- Mais fibra é normalmente melhor.
- Demasiada fibra pode causar inchaço, gás, e aumento dos movimentos intestinais.
- Há muitos factores que podem causar alterações epigenéticas, tais como fumar, exercício, stress, drogas, poluição, ou traumas.
- Os seus genes não são fixos e podem ser alterados pelas suas escolhas.
- Recomenda-se uma dieta rica em antioxidantes e fibras, evitando ao mesmo tempo a bioacumulação de agentes mutagénicos e toxinas numa cadeia alimentar.
- Dietas demasiado calóricas e desprovidas de nutrientes devem ser evitadase é recomendada a restrição calórica com jejum intermitente.
- A ingestão excessiva de proteínas pode exagerar o IGF1 e aumentar o risco de cancro.
Perguntas Frequentes
Referências:
- Peixoto, P., Cartron, P. F., Serandour, A. A., & Hervouet, E. (2020). De 1957 aos nossos dias: Uma Breve História da Epigenética. International journal of molecular ciências, 21(20), 7571. https://doi.org/10.3390/ijms21207571
- O que é a Epigenética? | CDC. (2022, 15 de agosto). Centros de Controlo e Prevenção de Doenças. https://www.cdc.gov/genomics/disease/epigenetics.htm
- LaPelusa, A., & Kaushik, R. (2022). Fisiologia, Proteínas. Em StatPearls. StatPearls Publishing. [PubMed]
- Blackwell, T. K., & Walker, A. K. (2006). Mecanismos de transcrição. WormBook : a revisão online da biologia de C. elegans, 1-16. https://doi.org/10.1895/wormbook.1.121.1
- Hamilton J. P. (2011). Epigenética: princípios e prática. Doenças digestivas (Basileia, Suíça), 29(2), 130-135. https://doi.org/10.1159/000323874
- Fanucchi, S., Domínguez-Andrés, J., Joosten, L. A. B., Netea, M. G., & Mhlanga, M. M. (2021). A interseção da epigenética e do metabolismo na imunidade treinada. Imunidade, 54(1), 32-43. https://doi.org/10.1016/j.immuni.2020.10.011
- Surace, A. E. A., & Hedrich, C. M. (2019). O papel da epigenética na doença autoimune / inflamatória. Fronteiras em imunologia, 10, 1525. https://doi.org/10.3389/fimmu.2019.01525
- Denhardt, D. T. (2018). Efeito do stress na biologia humana: Epigenética, adaptação, herança e significado social. Jornal de Fisiologia Celular, 233(3), 1975-1984. https://doi.org/10.1002/jcp.25837
- de Magalhães-Barbosa, M. C., Prata-Barbosa, A., & da Cunha, A. J. L. A. (2022). Stress tóxico, epigenética e desenvolvimento infantil. Jornal de pediatria, 98 Suplemento 1(Suplemento 1), S13-S18. https://doi.org/10.1016/j.jped.2021.09.007
- Cavalli, G., & Heard, E. (2019). Os avanços na epigenética ligam a genética ao ambiente e à doença. Natureza, 571(7766), 489-499. https://doi.org/10.1038/s41586-019-1411-0
- Brena, R. M., & Costello, J. F. (2007). Interações genoma-epigenoma no cancro. Genética molecular humana, 16 Spec n.º 1, R96-R105. https://doi.org/10.1093/hmg/ddm073
- Shen, H., & Laird, P. W. (2013). Interação entre o genoma do câncer e o epigenoma. Célula, 153(1), 38-55. https://doi.org/10.1016/j.cell.2013.03.008
- Hullar, M. A., & Fu, B. C. (2014). Dieta, o microbioma intestinal e epigenética. Revista sobre o cancro (Sudbury, Mass.), 20(3), 170-175. https://doi.org/10.1097/PPO.0000000000000053
- Abdul, Q. A., Yu, B. P., Chung, H. Y., Jung, H. A., & Choi, J. S. (2017). Modificações epigenéticas da expressão gênica por estilo de vida e meio ambiente. Arquivos de investigação farmacêutica, 40(11), 1219-1237. https://doi.org/10.1007/s12272-017-0973-3
- Catteau, A., & Morris, J. S. (2002). Metilação de BRCA1: um papel significativo no desenvolvimento de tumores? Seminários em Biologia do Cancro, 12(5), 359-371. https://doi.org/10.1016/s1044-579x(02)00056-1
- Prajzendanc, K., Domagała, P., Hybiak, J., Ryś, J., Huzarski, T., Szwiec, M., Tomiczek-Szwiec, J., Redelbach, W., Sejda, A., Gronwald, J., Kluz, T., Wiśniowski, R., Cybulski, C., Łukomska, A., Białkowska, K., Sukiennicki, G., Kulczycka, K., Narod, S. A., Wojdacz, T. K., Lubiński, J., ... Jakubowska, A. (2020). A metilação do promotor BRCA1 no sangue periférico está associada ao risco de câncer de mama triplo-negativo. Revista internacional do cancro, 146(5), 1293-1298. https://doi.org/10.1002/ijc.32655
- Yue, X., Zhao, Y., Xu, Y., Zheng, M., Feng, Z., & Hu, W. (2017). Mutante p53 no câncer: Acumulação, ganho de função e terapia. Revista de biologia molecular, 429(11), 1595-1606. https://doi.org/10.1016/j.jmb.2017.03.030
- Saliani, M., Jalal, R., & Javadmanesh, A. (2022). Análise da expressão diferencial de genes e RNAs longos não codificantes associados à mutação KRAS em células de câncer colorretal. Relatórios científicos, 12(1), 7965. https://doi.org/10.1038/s41598-022-11697-5
- Beetch, M., Harandi-Zadeh, S., Shen, K., Lubecka, K., Kitts, D. D., O'Hagan, H. M., & Stefanska, B. (2020). Os antioxidantes dietéticos remodelam os padrões de metilação do DNA em doenças crônicas. Jornal Britânico de Farmacologia, 177(6), 1382-1408. https://doi.org/10.1111/bph.14888
- Crider, K. S., Yang, T. P., Berry, R. J., & Bailey, L. B. (2012). Folato e metilação do DNA: uma revisão dos mecanismos moleculares e as evidências do papel do folato. Avanços na nutrição (Bethesda, Md.), 3(1), 21-38. https://doi.org/10.3945/an.111.000992
- Gensous, N., Franceschi, C., Santoro, A., Milazzo, M., Garagnani, P., & Bacalini, M. G. (2019). O impacto da restrição calórica nas assinaturas epigenéticas do envelhecimento. International journal of molecular ciências, 20(8), 2022. https://doi.org/10.3390/ijms20082022
- Choi, S. W., & Friso, S. (2010). Epigenética: Uma nova ponte entre nutrição e saúde. Avanços na nutrição (Bethesda, Md.), 1(1), 8-16. https://doi.org/10.3945/an.110.1004
- Borzabadi, S., Oryan, S., Eidi, A., Aghadavod, E., Daneshvar Kakhaki, R., Tamtaji, O. R., Taghizadeh, M., & Asemi, Z. (2018). Os efeitos da suplementação probiótica na expressão gênica relacionada à inflamação, insulina e lipídios em pacientes com doença de Parkinson: Um ensaio randomizado, duplo-cego e controlado por placebo. Arquivos da medicina iraniana, 21(7), 289-295. [PubMed]
- Ye, J., Wu, W., Li, Y., & Li, L. (2017). Influências da Microbiota Intestinal na Metilação do DNA e Modificação da Histona. Doenças digestivas e ciências, 62(5), 1155-1164. https://doi.org/10.1007/s10620-017-4538-6
- Bhattacharjee, S., & Dashwood, R. H. (2020). Regulação epigenética de NRF2 / KEAP1 por fitoquímicos. Antioxidantes (Basel, Suíça), 9(9), 865. https://doi.org/10.3390/antiox9090865
- Griñán-Ferré, Christian, et al. "Antioxidantes dietéticos, Epigenética e Envelhecimento Cerebral: Um enfoque no Resveratrol". Stress Oxidativo e Antioxidantes Dietéticos em Doenças Neurológicas, editado por Colin R. Martin e Victor R. Preedy, Academic Press, 2020, pp. 343-57 https://doi.org/10.1016/B978-0-12-817780-8.00022-0
- Chhabria, S. V., Akbarsha, M. A., Li, A. P., Kharkar, P. S., & Desai, K. B. (2015). Geração de alicina in situ usando entrega direcionada de alliinase para inibição de células MIA PaCa-2 por meio de alterações epigenéticas, estresse oxidativo e expressão do inibidor de quinase dependente de ciclina (CDKI). Apoptose : uma revista internacional sobre morte programada de células, 20(10), 1388-1409. https://doi.org/10.1007/s10495-015-1159-4
- Crider, K. S., Yang, T. P., Berry, R. J., & Bailey, L. B. (2012). Folato e metilação do DNA: uma revisão dos mecanismos moleculares e as evidências do papel do folato. Avanços na nutrição (Bethesda, Md.), 3(1), 21-38. https://doi.org/10.3945/an.111.000992
- Saitsu, H. (2017). Receptores de folato e fechamento do tubo neural. Anomalias congénitas, 57(5), 130-133. https://doi.org/10.1111/cga.12218
- Abraham, K. J., Ostrowski, L. A., & Mekhail, K. (2017). As moléculas de RNA não codificantes conectam a restrição calórica e a vida útil. Revista de biologia molecular, 429(21), 3196-3214. https://doi.org/10.1016/j.jmb.2016.08.020
- Patel, S. A., Velingkaar, N., Makwana, K., Chaudhari, A., & Kondratov, R. (2016). A restrição calórica regula a expressão do gene do relógio circadiano por meio de mecanismos dependentes e independentes de BMAL1. Relatórios científicos, 6, 25970. https://doi.org/10.1038/srep25970
- Gabandé-Rodríguez, E., Gómez de Las Heras, M. M., & Mittelbrunn, M. (2019). Controle da inflamação por miméticos de restrição calórica: Na encruzilhada da autofagia e da mitocôndria. Células, 9(1), 82. https://doi.org/10.3390/cells9010082
- Bagherniya, M., Butler, A. E., Barreto, G. E., & Sahebkar, A. (2018). O efeito do jejum ou restrição calórica na indução de autofagia: Uma revisão da literatura. Revisões da investigação sobre o envelhecimento, 47, 183-197. https://doi.org/10.1016/j.arr.2018.08.004
- Komatsu, T., Park, S., Hayashi, H., Mori, R., Yamaza, H., & Shimokawa, I. (2019). Mecanismos de restrição calórica: Uma revisão dos genes necessários para os efeitos de extensão da vida e inibição de tumores da restrição calórica. Nutrientes, 11(12), 3068. https://doi.org/10.3390/nu11123068
- Greger M. (2020). Uma dieta baseada em plantas de alimentos integrais é eficaz para a perda de peso: as evidências. Revista americana de medicina de estilo de vida, 14(5), 500-510. https://doi.org/10.1177/1559827620912400
- Makki, K., Deehan, E. C., Walter, J., & Bäckhed, F. (2018). O impacto da fibra dietética na microbiota intestinal na saúde e na doença do hospedeiro. Hospedeiro de célula e micróbio, 23(6), 705-715. https://doi.org/10.1016/j.chom.2018.05.012
Publicações Relacionadas
Você tem alguma dúvida sobre saúde e nutrição?
Eu adoraria ouvir de você e respondê-las em meu próximo post. Agradeço sua contribuição e opinião e espero ouvir de você em breve. Eu também convido você a siga-nos no Facebook, Instagram e Pinterest para mais conteúdos sobre dieta, nutrição e saúde. Pode deixar um comentário e ligar-se a outros entusiastas da saúde, partilhar as suas dicas e experiências e obter apoio e encorajamento da nossa equipa e comunidade.
Espero que este post tenha sido informativo e agradável para si e que esteja preparado para aplicar os conhecimentos que aprendeu. Se achou este post útil, por favor partilhá-lo com os seus amigos e familiares que também possam beneficiar com isso. Nunca se sabe quem poderá precisar de alguma orientação e apoio no seu percurso de saúde.
– Você Também Pode Gostar –

Aprender Sobre Nutrição
Milos Pokimica é médico de medicina natural, nutricionista clínico, escritor de saúde e nutrição médica, e conselheiro em ciências nutricionais. Autor da série de livros Go Vegan? Revisão de Ciênciaopera também o website de saúde natural GoVeganWay.com
Medical Disclaimer
GoVeganWay.com traz análises das pesquisas mais recentes sobre nutrição e saúde. As informações fornecidas representam a opinião pessoal do autor e não pretendem nem implicam substituir aconselhamento, diagnóstico ou tratamento médico profissional. As informações fornecidas são apenas para fins informativos e não se destinam a servir como substituto para consulta, diagnóstico e/ou tratamento médico de um médico ou profissional de saúde qualificado.NUNCA DESCONSIDERE o CONSELHO MÉDICO PROFISSIONAL OU adiar a BUSCA de TRATAMENTO MÉDICO por causa DE ALGO QUE TENHA LIDO OU ACESSADO por MEIO de GoVeganWay.com
NUNCA APLIQUE QUAISQUER MUDANÇAS de estilo de VIDA OU QUALQUER MUDANÇA COMO UMA CONSEQUÊNCIA DE ALGO QUE TENHA LIDO NO GoVeganWay.com ANTES de CONSULTORIA de LICENÇA MÉDICA.
No caso de uma emergência médica, ligue para o médico ou para o 911 imediatamente. GoVeganWay.com não recomenda ou endossa qualquer específicos, grupos, organizações, exames, médicos, produtos, procedimentos, opiniões ou outras informações que podem ser mencionadas dentro.
Sugestões do Editor –
Milos Pokimica é escritor especializado em saúde e nutrição e consultor em ciências nutricionais. Autor da série de livros Go Vegan? Revisão de Ciênciaopera também o website de saúde natural GoVeganWay.com
Artigos Mais Recentes -
Superior De Saúde De Notícias — ScienceDaily
- How often do people really fart? Scientists built smart underwear to find outon Março 14, 2026
Researchers have created “Smart Underwear,” a wearable device that measures flatulence by detecting hydrogen produced by gut microbes. Early tests suggest people may pass gas about 32 times a day—much higher than previous estimates. The device gives scientists a new way to track gut microbial activity in everyday life. It will power a new nationwide study called the Human Flatus Atlas to map normal patterns of gas production.
- Textbooks were wrong: Scientists reveal the surprising way human hair really growson Março 14, 2026
Hair may grow in a completely different way than scientists once believed. Instead of being pushed out from the root, new research shows that moving cells inside the follicle actually pull the hair upward like a microscopic motor. Advanced 3D imaging revealed a spiral movement of cells that generates this force. The finding could change how scientists study hair loss and design future treatments.
- A lab mistake at Cambridge reveals a powerful new way to modify drug moleculeson Março 14, 2026
Cambridge scientists have discovered a light-powered chemical reaction that lets researchers modify complex drug molecules at the final stages of development. Unlike traditional methods that rely on toxic chemicals and harsh conditions, the new approach uses an LED lamp to create essential carbon–carbon bonds under mild conditions. This could make drug discovery faster and more environmentally friendly. The breakthrough was uncovered unexpectedly during a failed laboratory experiment.
- Gut bacteria that make serotonin may hold the key to IBSon Março 14, 2026
Researchers have identified two gut bacteria that can produce serotonin, a key chemical that regulates bowel movements. In experiments with mice lacking serotonin, the microbes boosted serotonin levels, increased nerve cells in the colon, and normalized intestinal movement. The study also found that people with IBS have lower levels of one of these bacteria. The discovery suggests gut microbes could become a powerful new target for treating digestive disorders.
- Microplastics may be quietly damaging your brain and fueling Alzheimer’s and Parkinson’son Março 14, 2026
Tiny plastic particles may be quietly threatening brain health. New research suggests microplastics—now widely found in food, water, and even household dust—could trigger inflammation and damage in the brain through multiple biological pathways. Scientists estimate adults may consume about 250 grams of these particles each year, and some can accumulate in organs including the brain.
- Study finds two types of colon polyps can raise bowel cancer risk fivefoldon Março 13, 2026
Researchers studying over 8,400 colonoscopies discovered that having both adenomas and serrated polyps in the bowel can raise the risk of serious precancerous changes by up to five times. These two polyp types may represent separate cancer pathways that can occur at the same time. Nearly half of patients with serrated polyps also had adenomas, making this high-risk combination more common than expected. The results emphasize the importance of early detection and regular colonoscopy monitoring.
- Severe COVID or flu may raise lung cancer risk years lateron Março 13, 2026
A severe case of COVID-19 or influenza could increase the risk of lung cancer later on, according to new research. Scientists discovered that serious viral infections can alter immune cells in the lungs, leaving behind chronic inflammation that may help tumors develop months or years later. The increased risk was seen mainly after severe infections that required hospitalization. Vaccination, however, appears to prevent the dangerous lung changes.
PubMed, #vegan-dieta –
- Consumption Habits and Perception of Plant-Based Milk and Dairy Alternatives Among Vegetarians and Omnivores: A Case Study of Consumers in Sloveniaon Março 14, 2026
CONCLUSIONS: PBMDA perceptions in Slovenia are strongly segmented by dietary pattern and socio-demographics, supporting the need for clearer nutrition communication.
- Fatty acid composition of ground-beef products and their plant-based meat substitutes available in Hungaryon Março 13, 2026
CONCLUSION: The findings indicate that plant-based meat alternatives (except those containing coconut oil) have lower saturated and higher polyunsaturated fatty acid compositions than beef-based products, leading to more beneficial nutritional value. Further analytical and clinical studies are necessary to provide a more comprehensive understanding of the long-term health effects of these foods.
- Diet Modulates Cardiac Metabolic Stress During Anthracycline Treatmenton Março 12, 2026
Diet is a modifiable determinant of cardiovascular risk and may influence tolerance to cancer therapies. The mechanisms by which specific dietary components affect cardiac metabolism during anthracycline treatment remain poorly defined, limiting the incorporation of dietary recommendations into treatment guidelines. Here, we integrated heart proteomics data from patients treated with or without anthracyclines with a genome-scale reconstruction of human cardiac metabolism (CardioNet). Using…
- Sleeping green: an Italian survey for the assessment of the relationship between sleep and vegetarian dieton Março 10, 2026
CONCLUSION: Our findings suggest that an utterly veg diet can affect several sleep variables differently, mainly reducing the risk of OSA and increasing the frequency of hypnic jerks. We highlight the relevance of a thorough assessment of sleep measures associated with the veg diet and the importance of controlling for other confounding factors to reach a more nuanced understanding of the relationship between dietary patterns and sleep.
- Food sources of macro- and micronutrients in young children and adults following vegan, vegetarian, and omnivorous dietson Março 9, 2026
CONCLUSION: Consumption of fortified dairy and PBDA products was widespread and played an important role in supporting adequate nutrition across different diet groups. Greater attention should be given to dietary sources of iodine and long-chain n-3 fatty acids.
Postagens aleatórias –
Postagens em destaque –
Últimas do PubMed, #dieta baseada em vegetais –
- Adherence to Plant-Based Dietary Patterns and Digestive Cancers: A Scoping Reviewpor Alejandro Oncina-Cánovas on Março 14, 2026
Background/Objectives: Digestive cancers are among the leading causes of death worldwide. Although their etiology is not fully understood, diet is an important modifiable risk factor. This scoping review aimed to explore the existing evidence on the association between adherence to various plant-based dietary (PBD) patterns and the risk of major digestive cancers. Methods: The scoping review followed the Arksey and O’Malley framework and Joanna Briggs Institute recommendations, and results […]
- Consumption Habits and Perception of Plant-Based Milk and Dairy Alternatives Among Vegetarians and Omnivores: A Case Study of Consumers in Sloveniapor Kaja Kranjc on Março 14, 2026
CONCLUSIONS: PBMDA perceptions in Slovenia are strongly segmented by dietary pattern and socio-demographics, supporting the need for clearer nutrition communication.
- Diet Quality Is Not Associated with Malnutrition, Low Muscle Mass and Sarcopenia During Lung Cancer Treatment: A Cross-Sectional Studypor Annie R Curtis on Março 14, 2026
Background/Objectives: Studies evaluating the impact of diet quality on nutrition- and muscle-related outcomes in cancer are limited. This study aimed to understand the diet quality of people with lung cancer and its cross-sectional associations with malnutrition, low muscle mass and (probable)-sarcopenia. Methods: Three-day food records were collected from 47 adults (mean ± SD age 70.6 ± 8.6 years; 58% male) with lung cancer prior to, or within one week, of curative-intent […]
- Insulin Resistance and Platelet Hyperactivity: Hematological Insights and Nutritional Strategies for Vascular Protectionpor Kiana Mohammadian on Março 14, 2026
Insulin resistance (IR) promotes a prothrombotic milieu by enhancing platelet hyperactivity, oxidative stress, and endothelial dysfunction, driving both microvascular and macrovascular complications in type 2 diabetes. Our review synthesizes mechanistic evidence showing that insulin-resistant platelets exhibit increased basal activation, elevated sensitivity to agonists, and reduced responsiveness to inhibitory signals, with distinct pro-aggregatory subpopulations amplifying thrombotic risk….
- Relationship Between Diet Quality, Intestinal Permeability, and Gut Microbiota Features in Individuals with Obesitypor Sarah M Eaton on Março 14, 2026
Background/Objectives: This study examined relationships between diet quality, as determined using three a priori-defined dietary patterns (Healthy Eating Index of 2010 dietary guidelines [HEI-2010], Mediterranean Dietary Pattern [MDP], and Dietary Approaches to Stop Hypertension [DASH]), intestinal permeability, and features of the gut microbiota in a diverse, obese sample. Methods: This was a post hoc, cross-sectional study including 103 healthy, obese individuals (43.8 ± 11.3 years, BMI: […]
- Maternal Adherence to the Mediterranean Diet and Adverse Pregnancy Outcomes: Findings from the Multi-Center PLATONE Projectpor Simona Esposito on Março 14, 2026
Background/Objectives: Pregnancy is a critical period during which lifestyle factors, including diet, can affect maternal and fetal outcomes. The Mediterranean Diet (MD) may offer advantages, but evidence on its impact on adverse pregnancy outcomes is limited. We evaluated the association between an MD and adverse pregnancy outcomes, cesarean delivery, and stillbirth outcomes in a large sample of hospitalized women in Italy. Methods: A cross-sectional analysis of retrospectively assessed […]