Expression Génétique et Epigénétique : Comment l'Alimentation et l'Environnement Façonnent Votre Santé
Ce ne sont pas les gènes qui comptent, mais la façon dont ils s'expriment.
Milos Pokimica
Écrit par : Milos Pokimica
Examiné Médicalement Par : Dr. Xiùying Wáng, M.D.
Updated janvier 5, 2026Principaux Enseignements :
-L'expression génique et l'épigénétique sont des processus dynamiques et réactifs qui régulent la façon dont les gènes sont activés ou désactivés en réponse à divers stimuli.
-L'alimentation et l'environnement sont deux facteurs majeurs qui peuvent influencer l'expression des gènes et l'épigénétique, en fournissant des nutriments, des produits chimiques ou des signaux qui peuvent modifier l'ADN ou les protéines qui interagissent avec lui.
- Les changements dans l'expression des gènes peuvent avoir des effets significatifs sur la santé et la prévention des maladies, en modifiant les fonctions cellulaires, le métabolisme, l'inflammation, l'immunité et le vieillissement de l'organisme.
Introduction.
La plupart des gens connaissent dans une certaine mesure la science derrière la génétique. La génétique nous aide à comprendre comment fonctionne l'évolution et comment nous héritons des traits de nos parents et nous aide en médecine, ou anthropologie en comprenant comment nos corps ont évolué des hominines aux humains anatomiquement modernes.
Mais qu'en est-il épigénétique? Connaissez-vous ce terme ? Savez-vous que les gènes ne sont pas immuables ? Savez-vous comment nous pouvons changer notre destin en influençant nos gènes ? C'est un domaine scientifique nouveau et émergent de l'épigénétique.
Génétique classique.
Mais comment en sommes-nous arrivés là ? Comment avons-nous découvert les secrets de l'ADN et les mécanismes qui le régulent ?
Tout a commencé avec un moine nommé Gregor Mendel, qui a vécu au 19e siècle. Il était curieux de savoir comment les plantes héritaient de traits comme la couleur des fleurs et la forme des graines. Il a fait des expériences avec des plants de pois, les croisant et comptant la progéniture. Il a remarqué que certains traits suivaient de simples schémas d'héritage, tandis que d'autres semblaient se fondre ou disparaître. Il est venu avec quelques règles qui ont expliqué ses observations, que nous appelons maintenant les lois de l'héritage de Mendel. Il a publié son travail en 1865, mais personne ne s'en souciait. Il est mort sans savoir qu'il était le père du domaine scientifique le plus important appelé la génétique.
Avance rapide jusqu'au début du XXe siècle. Certains scientifiques ont redécouvert le travail de Mendel et réalisé que c'était du génie. Ils ont également découvert que les chromosomes étaient constitués d'ADN et de protéines et qu'ils portaient les unités d'héritage, qu'ils ont appelées gènes. Ils ont découvert comment les gènes étaient disposés sur les chromosomes, comment ils pouvaient être échangés pendant la méiose (division cellulaire) et comment ils pouvaient être mutés par des radiations ou des produits chimiques. Ils ont également appris à cartographier les gènes sur les chromosomes en utilisant l'analyse de liaison et les fréquences de recombinaison. C'était l'ère de la génétique classique.
Mais il y avait un problème. La génétique classique ne pouvait pas tout expliquer. Par exemple, comment les gènes contrôlent-ils les caractères ? Comment les gènes ont-ils interagi avec l'environnement ou dans quelle mesure celui-ci a-t-il un effet sur notre génome ? Comment les gènes ont-ils changé au fil du temps et d'une génération à l'autre ? Ces questions ont conduit à la création d'une nouvelle discipline appelée biologie moléculaire.
Dogme central.
En 1953, James Watson et Francis Crick ont résolu le structure de l'ADN. C'était une double hélice composée de quatre nucléotides (A, T, C, G) qui s'appariaient les uns aux autres de manière spécifique (A avec T, C avec G). Ils ont réalisé que cette structure expliquait comment l'ADN pouvait stocker des informations (la séquence de nucléotides), se copier (en séparant les brins et en les utilisant comme matrices) et s'exprimer (en étant transcrit en ARN et traduit en protéines). Ce travail est devenu le "dogme central de la biologie moléculaire”. Une théorie affirme que l'information génétique ne circule que dans une seule direction, de l'ADN à l'ARN, à la protéine ou de l'ARN directement à la protéine. Il a été énoncé pour la première fois par Francis Crick en 1957 et publié en 1958.
Mais il y avait un autre problème. La biologie moléculaire ne pouvait pas non plus tout expliquer.
Par exemple, comment les cellules savaient-elles quand et où activer et désactiver les gènes ? Au cours du développement, comment les cellules se sont-elles divisées en types distincts parce que chacune a le même ADN ? Comment les cellules se sont-elles souvenues de leur identité et de leur histoire, ce qui est important pour la recherche sur le cancer ? Comment les cellules ont-elles répondu aux signaux d'autres cellules ou de l'environnement ?
Naissance de l'épigénétique.
Ces questions ont conduit à la naissance de l'épigénétique, qui visait à révéler les mécanismes qui régulent l'expression des gènes sans modifier la séquence d'ADN.
Le terme épigénétique a été inventé par Conrad Waddington en 1942, mais il a fallu des décennies pour qu'il soit accepté par la science.
L'épigénétique repose sur l'idée qu'il existe des modifications chimiques sur l'ADN ou sur histones (protéines qui s'enroulent autour de l'ADN) qui peuvent affecter la manière dont les gènes sont accessibles et utilisés par la machinerie cellulaire. Ces modifications peuvent être ajoutées ou supprimées par des enzymes, en fonction de divers facteurs tels que le type de cellule, le stade de développement, les signaux environnementaux, le stress, l'alimentation, etc. (Peixoto et al., 2020). Ces changements peuvent également être transmis aux cellules filles lors de la division cellulaire, voire aux enfants lors de la reproduction.
Cela signifie que l'épigénétique peut influencer des traits qui ne sont pas codés par l'ADN seul, tels que le comportement, la susceptibilité aux maladies ou le vieillissement.
L'épigénétique est l'un des sujets les plus brûlants, tout comme la génétique l'était encore plus. Le problème est que la plupart des gens n'en ont pas entendu parler, de sorte que la vieille croyance demeure que les gènes sont tout. Nous devons populariser la nouvelle recherche auprès du grand public qui croit toujours que les gènes sont gravés dans le marbre et qu'il n'y a rien que vous puissiez y faire. L'épigénétique remet en question certaines des hypothèses et des dogmes de la génétique et de la biologie moléculaire. Il ouvre de nouvelles possibilités pour comprendre la vie à un niveau plus profond. Elle ouvre également de nouvelles voies pour améliorer la médecine et la santé en modifiant l'expression des gènes.
Ce ne sont pas les gènes qui comptent, mais la façon dont ils s'expriment.
Qu'est-ce que l'expression génique ?
Avant de nous plonger plus scientifiquement dans l'épigénétique, parlons de l'expression des gènes.
L'expression des gènes fait référence à la fréquence ou au moment où les protéines sont créées à partir des instructions contenues dans les gènes. (What Is Epigenetics? | CDC, 2022b).
Les protéines sont des éléments constitutifs. Elles remplissent de nombreuses fonctions, telles que la construction des tissus, la lutte contre les infections et la régulation des hormones (Pelusa et al., 2022).
Vos gènes portent les informations nécessaires à la production de protéines, mais ils ne produisent pas eux-mêmes de protéines. Ils ont besoin de l'aide d'autres molécules, comme ARN et des enzymes, pour lire le code et produire les protéines. Ce processus est appelé transcription (Blackwell et al., 2006).
La transcription n'est pas toujours activée. Il peut être activé ou désactivé en fonction de différents facteurs, tels que des signaux provenant d'autres cellules, des hormones ou des nutriments. C'est ainsi que notre corps s'adapte à différentes situations.
Par exemple, lorsque vous avez faim, votre corps active des gènes qui font que les enzymes décomposent les aliments et libèrent de l'énergie. Lorsque vous êtes rassasié, votre corps désactive ces gènes et active les gènes qui stockent l'excès d'énergie sous forme de graisse.
Pourquoi l'épigénétique est-elle importante ?
Epi signifie au-dessus ou "au-dessus de" en grec. Ce ne sont pas vos gènes qui comptent, mais ce qu'ils expriment.
Toutes vos cellules ont les mêmes gènes mais ont un aspect et un comportement différents en raison de changements épigénétiques. En d'autres termes, il s'agit d'une couche d'information supplémentaire qui contrôle la régulation des gènes (Hamilton et al., 2011).
Les modifications épigénétiques peuvent inhiber ou activer l'expression des gènes. La combinaison de ces modifications joue un rôle important dans l'"empreinte", une sorte de "marque" qui détermine si un gène sera exprimé ou non.
L'ADN est formé par des combinaisons de nucléotides. Ce sont les lettres célèbres que la plupart des gens connaissent, adénine (A), thiamine (T), guanine (G) et cytosine (C).
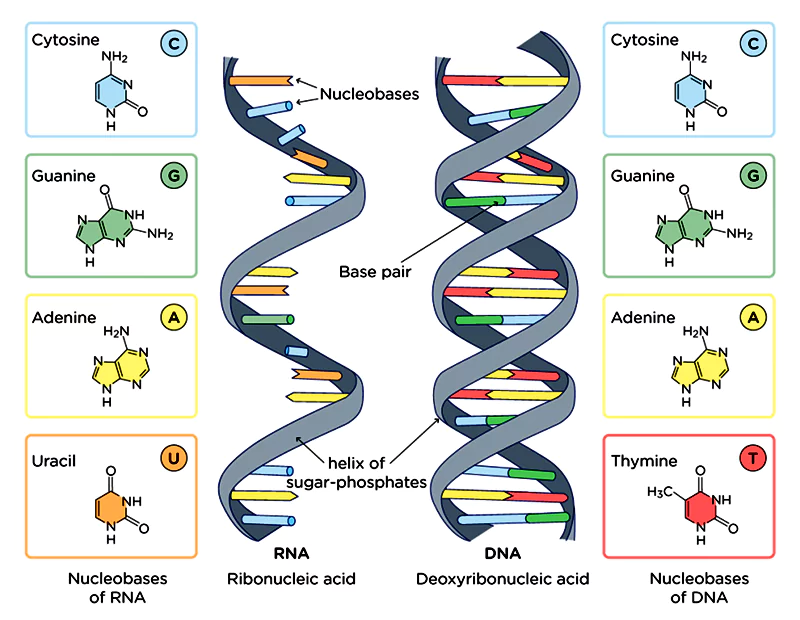
La cytosine, par exemple, peut être modifiée en ajoutant un groupe méthyle (CH3).
Ce processus est connu sous le nom de méthylation et modifie l'expression du gène dont la séquence a été modifiée. La méthylation de l'ADN conduit généralement au silence du gène. Dans de mauvaises circonstances, cela pourrait être très mauvais si le gène régule le système immunitaire ou une autre fonction importante.
Les changements épigénétiques peuvent se produire avant même votre naissance, pendant votre développement et tout au long de votre vie. Certains changements épigénétiques sont normaux et nécessaires à votre croissance et à votre fonction.
D'autres changements épigénétiques sont influencés par vos comportements et votre environnement.
Par exemple, ce que vous mangez peut affecter la façon dont vos gènes sont méthylés ou dont vos histones sont modifiées.
Votre activité physique peut affecter la quantité d'ARN non codant produite ou son interaction avec l'ARN codant.
Ces changements épigénétiques font partie de l'évolution et ont leur raison d'être mais aussi dans certains scénarios peuvent avoir des effets positifs ou négatifs sur votre santé.
Certains changements épigénétiques, par exemple, peuvent améliorer notre système immunitaire en activant des gènes qui combattent l'inflammation ou le cancer.
D'autres modifications épigénétiques peuvent augmenter le risque de maladies en désactivant des gènes qui régulent le métabolisme ou le système immunitaire (Fanucchi et al, 2021); (Surace et al., 2019).
C'est un moteur d'adaptation et d'évolution. Si vous voulez une preuve de l'évolution et de son fonctionnement en temps réel et de la façon dont les organismes évoluent, c'est tout. C'est une raison pour laquelle les changements épigénétiques peuvent également être hérités d'une génération à l'autre. Par exemple, si vos grands-parents ont été exposés à des toxines, à des agents mutagènes ou à des facteurs de stress et que cette exposition a entraîné des modifications épigénétiques de leur ADN, de leurs spermatozoïdes ou de leurs ovules, ces modifications pourraient vous être transmises et affecter l'expression de vos gènes (Denhardt et al., 2018).
Un environnement pollué et des toxines omniprésentes n'affecteront pas seulement votre ADN, mais aussi celui de vos enfants (de Magalhães-Barbosa et al., 2022).
Changements épigénétiques et leurs effets sur la santé.
Le tableau ci-dessous illustre les principaux facteurs qui influencent l'expression des gènes et les changements épigénétiques. Il y a plus de facteurs, mais ce que vous pouvez retenir de ce tableau, c'est le fait que dans chaque ligne, les facteurs qui influencent le risque sont l'alimentation, le stress et l'exposition aux toxines.
| Changements épigénétiques | Effets sur la santé | Sources |
| Méthylation de l'ADN | Processus qui ajoute des groupes méthyles aux bases de l'ADN, affectant ainsi l'expression des gènes. Les variables environnementales telles que l'alimentation, le stress et les exposition à la toxicité peuvent tous altérer la méthylation de l'ADN. La méthylation de l'ADN peut affecter divers aspects de la santé, tels que le risque de cancer, la fonction immunitaire et le vieillissement. | Cavalli et al., 2019 |
| Modifications des histones | Un processus qui modifie la structure des histones, les protéines qui s'enroulent autour de l'ADN. Les modifications des histones peuvent affecter la façon dont l'ADN est étroitement ou lâchement emballé, affectant l'expression des gènes. Les modifications des histones peuvent être influencées par des facteurs environnementaux tels que l'alimentation, le stress et l'exposition aux toxines. Les modifications des histones peuvent affecter divers aspects de la santé, tels que le risque de cancer, la fonction immunitaire et le vieillissement. | Cavalli et al., 2019 |
| ARN non codant | ARN qui ne code pas pour les protéines. Des facteurs environnementaux tels que l'alimentation, le stress et l'exposition aux toxines peuvent tous affecter l'ARN non codant. L'ARN non codant peut avoir un impact sur de nombreux domaines de la santé, notamment le risque de cancer, la fonction immunologique et le vieillissement. | Cavalli et al., 2019 |
| infections | Les germes peuvent modifier votre épigénétique pour affaiblir votre système immunitaire. Cela aide le germe à survivre. Exemple : Mycobacterium tuberculosis provoque la tuberculose. La tuberculose était et pourrait toujours être une maladie mortelle car elle peut altérer la méthylation de l'ADN des cellules immunitaires, rendant ainsi le système immunitaire moins efficace pour combattre l'infection. | What Is Epigenetics? | CDC, 2022b |
Exemples de changements épigénétiques et leurs effets sur le risque de cancer.
Le cancer est une maladie complexe qui implique des milliers de mutations différentes qui s'accumulent et des changements dans le génome et l'épigénome (Brena et al., 2007), (Shen et al., 2013). On peut avoir une prédisposition génétique à être endurci par ses parents, mais ce n'est qu'une partie de l'ensemble du tableau.
Cette prédisposition génétique au cancer s'active en fait en fonction de l'expression des gènes et cette expression dépend principalement d'un régime alimentaire (Hullar et al., 2014), et l'environnement (Abdul et al., 2017).
Les changements épigénétiques peuvent activer ou désactiver des gènes impliqués dans la croissance cellulaire, la mort cellulaire ou la réponse immunitaire. Ces changements peuvent alors affecter votre risque global de développer un cancer ou de répondre au traitement du cancer. C'est pourquoi nous avons une épidémie de cancer où une personne sur quatre dans les sociétés occidentales avec un régime alimentaire américain standard en mourra. Ce ne sont pas les mauvais gènes qui en sont la cause, mais l'expression des gènes.
Voici quelques exemples de changements épigénétiques et leurs effets sur le risque de cancer :
- La méthylation de l'ADN empêche les protéines qui lisent le gène d'y accéder, ce qui revient à désactiver le gène. La méthylation de l'ADN peut désactiver les gènes qui suppriment les tumeurs ou réparent les dommages causés à l'ADN, désactivant ainsi le système immunitaire. Par exemple, une mutation du gène BRCA1 qui l'empêche de fonctionner correctement augmente le risque de cancer du sein et d'autres types de cancer. Toutefois, si ce gène est également méthylé, vous mourrez très probablement parce que votre système immunitaire est désactivé. La méthylation peut encore augmenter votre risque de cancer et rendre votre cancer plus agressif (Catteau et al., 2002), (Prajzendanc et al., 2020).
- La modification des histones se produit lorsque des groupes chimiques sont ajoutés ou retirés des histones, qui sont des protéines qui s'enroulent autour de l'ADN pour former une structure appelée chromatine. Selon le type et l'emplacement des groupes chimiques, la modification des histones peut rendre la chromatine plus serrée ou plus lâche, affectant la quantité d'ADN exposée ou cachée des protéines qui la lisent. La modification des histones peut affecter les gènes qui régulent le cycle cellulaire, l'apoptose ou l'angiogenèse. Par exemple, une mutation du gène p53 qui l'empêche de fonctionner correctement vous rend plus susceptible de contracter divers cancers. Cependant, si ce gène est également modifié par des histones, il peut encore augmenter votre risque de cancer ou rendre votre cancer plus résistant au traitement (Yue et al., 2017).
- ARN non codant : C'est à ce moment que des molécules appelées ARN non codant se fixent à l'ARN codant, qui est utilisé pour fabriquer des protéines. L'ARN non codant peut aider à décomposer l'ARN codant ou à recruter des molécules qui modifient les histones, affectant l'expression des gènes. L'ARN non codant peut affecter les gènes qui contrôlent la différenciation, l'invasion ou les métastases cellulaires. Par exemple, une mutation du gène KRAS qui l'empêche de fonctionner correctement vous rend plus susceptible d'avoir un cancer colorectal. Cependant, si ce gène est également régulé par de l'ARN non codant, il peut encore augmenter votre risque de cancer ou rendre votre cancer plus difficile à traiter (Saliani et al., 2022).
Changements épigénétiques et leurs effets en fonction du régime alimentaire et de la nutrition
| Composants alimentaires | Changements épigénétiques | Sources |
| Antioxydants | Les antioxydants sont des molécules capables de neutraliser les radicaux libres, ce qui peut endommager l'ADN et les histones. Les antioxydants peuvent moduler les changements épigénétiques en affectant la méthylation de l'ADN et les modifications des histones. | Beetch et al., 2020 |
| Folate | Le folate est une vitamine B impliquée dans la synthèse de l'ADN et de l'ARN. Le folate peut affecter les changements épigénétiques en fournissant des groupes méthyle pour la méthylation de l'ADN. Une carence en folate peut altérer la méthylation de l'ADN et augmenter le risque de diverses maladies, telles que le cancer, les anomalies du tube neural et les troubles cognitifs. | Crider et al., 2012 |
| Restriction calorique | La restriction calorique est une intervention diététique qui réduit l'apport calorique sans provoquer de malnutrition par la régulation à la baisse de divers facteurs, tels que l'inflammation, le stress oxydatif et le taux métabolique de base. La restriction calorique peut affecter les changements épigénétiques en modifiant l'expression et l'activité des enzymes impliquées dans la méthylation de l'ADN et les modifications des histones. | Gensous et al., 2019 |
| Fibre | La fibre est un type de glucide qui n'est pas digéré par les enzymes humaines mais qui peut être fermenté par les bactéries intestinales. Les fibres peuvent affecter les changements épigénétiques en influençant la composition et la fonction du microbiote intestinal, qui peut produire des métabolites qui modulent la méthylation de l'ADN et les modifications des histones. | Choi et al., 2010 |
| Probiotiques | Les probiotiques peuvent affecter les changements épigénétiques en influençant la composition et la fonction du microbiote intestinal, qui peut produire des métabolites qui modulent la méthylation de l'ADN et les modifications des histones. Les probiotiques peuvent également moduler l'expression de gènes impliqués dans l'inflammation, l'immunité et le métabolisme. | (Borzabadi et al., 2018), (Ye et al., 2017) |
| Prébiotiques | Les prébiotiques sont des glucides non digestibles qui stimulent de manière sélective la croissance et/ou l'activité des bactéries intestinales bénéfiques. Les prébiotiques peuvent affecter les changements épigénétiques en influençant la composition et la fonction du microbiote intestinal, qui peut produire des métabolites qui modulent la méthylation de l'ADN et les modifications des histones. Les prébiotiques peuvent également moduler l'expression de gènes impliqués dans l'inflammation, l'immunité et le métabolisme. | Ye et al., 2017 |
Effet des antioxydants sur l'expression des gènes.
Voici quelques exemples, ce n'est pas une liste complète de tous les effets, juste un exemple :
- Les antioxydants peuvent empêcher ou inverser la méthylation de l'ADN. La méthylation de l'ADN peut se produire lorsque vous êtes exposé à des radicaux libres ou à des toxines. Les antioxydants peuvent bloquer ce processus ou éliminer le groupe méthyle, restaurant la fonction du gène.
- Les antioxydants peuvent moduler les modifications des histones. Les antioxydants peuvent influencer les enzymes qui effectuent ces modifications, modifiant la structure de la chromatine.
- Les antioxydants peuvent réguler l'ARN non codant. Les antioxydants peuvent affecter la production ou l'activité de l'ARN non codant, altérant la régulation des gènes.
- Les antioxydants peuvent prévenir ou réparer les dommages à l'ADN et restaurer l'expression normale des gènes, empêchant ou ralentissant le développement du cancer.
Dans le tableau ci-dessous sont sélectionnés des antioxydants et leurs effets sur l'expression des gènes. Ce n'est pas une liste complète, juste quelques exemples qui ont été étudiés par le scientifique. Il y a des milliers de composés phytochimiques différents et vous devriez ou ne pourriez pas tous les rechercher. Vous devez vous efforcer d'augmenter valeur ORAC globale de votre alimentation par la nutrition et ne pas suivre la voie des antioxydants supplémentaires individuels. Les composés phytochimiques agissent en synergie comme un complexe de produits chimiques provenant de sources alimentaires entières où 2 plus 2 égalent 15. Dans le tableau, j'ai énuméré certains antioxydants à titre d'exemple.
| Antioxydant | Effet sur l'épigénétique | Source |
| Curcumine | La curcumine est un polyphénol anti-inflammatoire, antioxydant et anticancéreux produit à partir du curcuma. La curcumine peut inhiber les ADN méthyltransférases (DNMT) et les histones désacétylases (HDAC), provoquant la réactivation des gènes suppresseurs de tumeurs et la suppression des oncogènes. La curcumine peut également modifier la structure de la chromatine et l'expression des gènes en induisant l'acétylation et la méthylation des histones. La curcumine peut moduler les microARN (miARN) et les longs ARN non codants (lncARN), qui ciblent tous deux des gènes impliqués dans l'inflammation, l'apoptose, le cycle cellulaire, l'invasion et les métastases. | Bhattacharjee et al., 2020 |
| Resvératrol | Le resvératrol est un polyphénol naturel présent dans le raisin, le vin rouge, les baies et les cacahuètes qui a des effets antioxydants, anti-inflammatoires et anticancéreux. Le resvératrol peut inhiber les DNMT et les HDAC, entraînant la déméthylation et la réactivation des gènes suppresseurs de tumeurs et la régulation à la baisse des oncogènes. Le resvératrol peut également induire l'acétylation et la méthylation des histones, affectant la structure de la chromatine et l'expression des gènes. Le resvératrol peut réguler les miARN et les lncARN qui ciblent les gènes impliqués dans le stress oxydatif, l'inflammation, l'apoptose, l'autophagie, la sénescence, l'angiogenèse et les métastases. | Griñán-Ferré et al., 2020 |
| Apigénine | L'apigénine est un flavonoïde naturel dérivé des fleurs de camomille, des oranges, du persil, du céleri et d'autres sources naturelles qui possède des propriétés antioxydantes, anti-inflammatoires et anticancéreuses. L'apigénine peut inhiber les DNMT et les HDAC, entraînant la déméthylation et la réactivation des gènes suppresseurs de tumeurs et la régulation à la baisse des oncogènes. L'apigénine peut également induire l'acétylation et la méthylation des histones, modifiant la structure de la chromatine et l'expression des gènes. L'apigénine peut réguler les miARN qui ciblent les gènes impliqués dans le cycle cellulaire, l'apoptose, l'invasion, les métastases, l'angiogenèse et la souche. | Bhattacharjee et al., 2020 |
| Sulforaphane | Le sulforaphane est un isothiocyanate naturel dérivé de légumes crucifères tels que le brocoli, le chou et le chou frisé qui ont des propriétés antioxydantes, anti-inflammatoires et anticancéreuses. Le sulforaphane peut inhiber les DNMT et les HDAC, entraînant la déméthylation et la réactivation des gènes suppresseurs de tumeurs et la régulation à la baisse des oncogènes. Le sulforaphane peut également induire l'acétylation et la méthylation des histones, altérant la structure de la chromatine et l'expression des gènes. Le sulforaphane peut réguler les miARN et les lncARN qui ciblent les gènes impliqués dans l'inflammation, l'apoptose, le cycle cellulaire, l'invasion et les métastases. | Bhattacharjee et al., 2020 |
| Acide ursolique | L'acide ursolique est un triterpénoïde pentacyclique naturel présent dans divers fruits, herbes et épices qui a des effets antioxydants, anti-inflammatoires et anticancéreux. L'acide ursolique peut inhiber les DNMT et les HDAC, entraînant la déméthylation et la réactivation des gènes suppresseurs de tumeurs et la régulation à la baisse des oncogènes. L'acide ursolique peut également induire l'acétylation et la méthylation des histones, affectant la structure de la chromatine et l'expression des gènes. L'acide ursolique peut réguler les miARN qui ciblent les gènes impliqués dans le cycle cellulaire, l'apoptose, l'invasion, les métastases, l'angiogenèse et la souche. | Bhattacharjee et al., 2020 |
| Allicine | L'allicine est un composé soufré naturel dérivé de ail qui a des effets antimicrobiens, antioxydants, anti-inflammatoires et anticancéreux. L'allicine peut inhiber l'activité de l'ADN gyrase chez les bactéries, entraînant l'inhibition de la réplication et de la transcription de l'ADN. L'allicine peut également oxyder les résidus de cystéine dans les protéines, affectant leur structure et leur fonction. L'allicine peut réguler les miARN qui ciblent les gènes impliqués dans le cycle cellulaire, l'apoptose, l'invasion, les métastases, l'angiogenèse et la souche. | Chhabria et al., 2015 |
Il existe de nombreux autres antioxydants qui peuvent affecter l'expression des gènes. Si vous souhaitez en savoir plus, vous pouvez rechercher des articles corrélés.
Vous vous demandez peut-être aussi d'où vous pouvez vous procurer des antioxydants. La bonne nouvelle est qu'ils se trouvent principalement dans les plantes et qu'il existe des plantes très riches en antioxydants. Apprenez vos valeurs ORAC.
Effets du folate sur l'expression des gènes.
Le folate est une vitamine B impliquée dans la synthèse de l'ADN et de l'ARN. Vous avez besoin de folate pour que vos cellules se développent et se divisent correctement. Vous pouvez obtenir du folate à partir d'aliments comme les légumes-feuilles, les haricots, les noix, les œufs et les céréales enrichies. Le problème est que c'est l'un des plus répandus carences dans le régime américain standard. Les personnes qui suivent un régime alimentaire complet à base de plantes ne manquent généralement pas de folate et n'ont pas besoin d'un supplément supplémentaire d'acide folique.
Voici quelques exemples :
- Les folates fournissent des groupes méthyles (un groupe de carbone) pour la méthylation de l'ADN (Crider et al., 2012). Le folate est l'une des principales sources de groupes méthyles pour ce processus. Une carence en folate peut altérer la méthylation de l'ADN et provoquer une expression génique anormale.
- Les folates affectent la fermeture du tube neural. Le tube neural est la structure qui forme le cerveau et la moelle épinière de l'embryon. Le tube neural doit se fermer correctement pour un développement normal. Le folate est essentiel à ce processus car il affecte l'expression des gènes impliqués dans la fermeture du tube neural (Saitsu et al., 2017). Une carence en folate peut empêcher la fermeture du tube neural et provoquer des malformations congénitales telles que le spina bifida.
- Le folate est important pour la fonction cognitive car il affecte l'expression des gènes impliqués dans le développement et le fonctionnement du cerveau. Une carence en folate peut altérer la fonction cognitive et augmenter le risque de démence.
Voici quelques-uns des effets du folate sur l'épigénétique et pourquoi ils sont importants pour votre santé et votre développement. Vous vous demandez peut-être de quelle quantité de folate vous avez besoin et où vous pouvez vous en procurer. Eh bien, voici quelques conseils :
- Le RDA pour le folate est de 400 microgrammes pour les adultes et de 600 mcg pour les femmes enceintes.
- Vous pouvez obtenir du folate à partir d'aliments tels que les légumes-feuilles, les haricots, les noix, les œufs et les céréales enrichies. Vous pouvez également prendre un supplément si vous avez une carence ou un besoin plus important en folate.
- Vous devez éviter de prendre trop de folate car cela peut masquer une vitamine Carence en B12 ou interférer avec certains médicaments.
- De plus, l'acide folique n'est pas le même que le folate. Nous avons besoin de folate mais les suppléments sont faits d'acide folique. Contrairement au foie des rats du modèle animal, notre foie est incapable de convertir plus de 400 mg d'acide folique en folate en une journée. C'est pourquoi la plupart des suppléments ne dépassent jamais plus de 400 mg d'acide folique.
Effets de la restriction calorique sur l'expression des gènes.
La restriction calorique consiste à réduire l'apport calorique sans provoquer de malnutrition. La restriction calorique peut affecter la quantité d'ARN non codant produite ou la manière dont il interagit avec l'ARN codant (Abraham et all., 2017). La restriction calorique peut également réguler le rythme circadien de l'expression des gènes dans différents organes et tissus (Patel et al., 2016).
Ces effets de la restriction calorique sur l'épigénétique peuvent avoir divers avantages pour votre santé et votre vieillissement. Par exemple :
- La restriction calorique peut ralentir le vieillissement en modulant diverses voies, telles que l'inflammation (Gabandé-Rodríguez et al., 2019), le stress oxydatif, le métabolisme et l'autophagie (Bagherniya et al., 2018).
- La restriction calorique peut également prolonger la durée de vie en augmentant l'expression des gènes qui protègent contre les dommages cellulaires et la mort (Komatsu T et al., 2019).
Dans notre évolution normale, nous avons été contraints à des restrictions caloriques dans notre environnement normal pour tous nos ancêtres hominidés en raison de la rareté. La réponse de notre corps à la restriction est de se réparer en détruisant les mauvaises cellules, les cellules mutées ou les cellules précancéreuses, d'abord pour obtenir de l'énergie, et en ralentissant le métabolisme. Lorsque vous ralentissez votre métabolisme, vous brûlez moins d'énergie, vous avez moins de stress oxydatif et vous vivez plus longtemps. La restriction calorique a également des effets sur l'expression des gènes. Notre corps est habitué à l'autophagie et s'attend à ce qu'elle fasse partie intégrante de la vie. Un manque d'autophagie entraîne directement un risque de cancer. A le régime alimentaire complet à base de plantes est naturellement plus enclin à induire une restriction calorique en apportant moins de calories qu'un régime américain standard (SAD) tout en répondant aux besoins nutritionnels (Grégoire, 2020). La dépression saisonnière, quant à elle, entraîne un excès de calories dû à la consommation d'huile, de sucre et d'aliments très appétissants, ce qui peut nuire à l'expression des gènes et augmenter le risque de maladie.
Effets des fibres sur l'expression des gènes.
La fibre est un type de glucide qui n'est pas directement digéré par nos enzymes mais qui se retrouve dans le côlon où il est fermenté par les bactéries intestinales. Les fibres peuvent vous aider à réguler votre digestion, à réduire votre cholestérol et à prévenir la constipation.
Les bactéries qui fermentent les fibres sont symbiotiques et bonnes pour notre système immunitaire et notre corps, contrairement aux bactéries non probiotiques qui putréfient la viande. Cette bactérie mangeuse de viande putréfie la chair que vous avez mangée pendant des heures dans le côlon, provoquant une inflammation. La viande est la viande et la vôtre est savoureuse aussi.
Vous pouvez obtenir des fibres à partir d'aliments comme les fruits, les légumes, les céréales, les haricots et les noix.
Voici quelques exemples :
- Les fibres peuvent affecter la composition et la fonction du microbiote intestinal en fournissant de la nourriture aux bactéries probiotiques et en stimulant leur croissance et leur activité contre les bactéries non probiotiques mangeuses de viande (Makki et al., 2018).
- Les fibres affectent les métabolites produits par le microbiote intestinal. Les métabolites sont les substances produites ou consommées par le microbiote intestinal. Ils peuvent pénétrer dans la circulation sanguine et affecter les organes et les tissus. Les fibres peuvent influencer le type et la quantité de ces métabolites produits par le microbiote intestinal en stimulant les bactéries probiotiques et en régulant à la baisse les processus métaboliques des bactéries non probiotiques mangeuses de viande dans le côlon (Makki et al., 2018).
- Ces métabolites peuvent alors affecter la régulation épigénétique en modulant la disponibilité ou l'activité de donneurs chimiques ou d'enzymes qui contrôlent la méthylation de l'ADN et les modifications des histones. Ces modifications épigénétiques peuvent altérer l'expression de gènes impliqués dans l'inflammation, l'immunité et le métabolisme.
- Les fibres peuvent protéger contre l'obésité et le diabète en modulant l'expression de gènes impliqués dans l'homéostasie du glucose, le métabolisme des lipides et la dépense énergétique.
- Les fibres peuvent améliorer la fonction immunitaire. L'inflammation chronique peut être la conséquence d'un déséquilibre du microbiote intestinal ou d'une altération de la fonction barrière de l'intestin. Les fibres peuvent améliorer la fonction immunitaire et prévenir les infections en modulant l'expression des gènes impliqués dans l'inflammation, l'immunité et la fonction de barrière et en régulant à la baisse l'activité et le nombre de bactéries non probiotiques dans la colonie du microbiote. Les fibres peuvent également stimuler la production d'anticorps et de cytokines qui aident à combattre les germes..
L'apport alimentaire recommandé (AJR) pour les fibres est de 25 grammes par jour pour les femmes et de 38 grammes par jour pour les hommes. C'est juste RDA pour SAD. Dans un sens anthropologique, nos ancêtres hominidés ont consommé bien plus que cela. Une règle avec la fibre est que plus c'est généralement mieux. Le problème est que nous ne voulons pas de ballonnements, de gaz et de selles en constante augmentation. Nous n'aimons pas non plus la texture funky de la fibre sans goût, nous préférons donc ne pas la manger.
Dans la vidéo ci-dessous, Oded Rechavi, Ph.D., professeur de neurobiologie à l'Université de Tel Aviv et expert sur la façon dont les gènes sont hérités, comment les expériences façonnent les gènes, et remarquablement, comment certains souvenirs d'expériences peuvent être transmis via les gènes à la progéniture. Il discute de sa recherche qui remet en question les principes de longue date de l'héritage génétique et de la pertinence de ces découvertes pour comprendre les processus biologiques et psychologiques clés, notamment le métabolisme, le stress et les traumatismes. Il décrit l'histoire de l'exploration scientifique de «l'héritabilité des traits acquis» et comment l'épigénétique et la biologie de l'ARN peuvent expliquer en partie le passage de certains souvenirs basés sur l'expérience.
Conclusion :
Il s'agit d'un vaste sujet qui est au premier plan de la recherche scientifique au cours des deux dernières décennies. J'ai essayé de donner un résumé dans cet article avant d'aborder certains scénarios spécifiques dans des articles corrélés.
Ce ne sont là que quelques exemples de changements épigénétiques et de leurs effets sur le risque de cancer. De nombreux autres facteurs peuvent provoquer des changements épigénétiques, tels que le tabagisme, l'exercice, le stress, les drogues, la pollution ou les traumatismes.
L'essentiel est que vos gènes ne sont pas fixes. Vous pouvez les modifier selon vos choix et vous devez choisir une alimentation riche en antioxydants et en fibres, évitant la bioaccumulation de mutagènes et de toxines dans une chaîne alimentaire. Vous devez éviter les types de régimes trop caloriques et denses dépourvus de nutriments et incorporer la restriction calorique avec le jeûne intermittent et éviter de surexprimer votre système endocrinien avec un apport excessif en protéines. Il y a un niveau élevé de corrélation entre le risque global de cancer et des niveaux chroniquement élevés d'IGF-1 (en raison d'un régime SAD de haute qualité dominé par des protéines).

Faites donc des choix intelligents qui protègent l'expression de vos gènes et réduisent votre risque de cancer. Mon conseil est de ne pas attendre cinquante ans de plus avant que les recommandations ne changent, comme nous l'avons fait avec le tabagisme. Vous avez le pouvoir de changer non seulement vos gènes, mais également les gènes de vos enfants.
- La génétique classique ne pouvait pas tout expliquer, conduisant à la création de la biologie moléculaire.
- L'épigénétique a défié les hypothèses et les dogmes de la génétique et de la biologie moléculaire.
- L'épigénétique expose les mécanismes qui régulent l'expression des gènes sans modifier la séquence d'ADN.
- Ce ne sont pas les gènes qui comptent, mais la façon dont ils s'expriment.
- Les modifications chimiques sur l'ADN ou les histones peuvent affecter la façon dont les gènes sont accessibles et utilisés.
- Des modifications peuvent être ajoutées ou supprimées par des enzymes en fonction de divers facteurs.
- Les changements peuvent être transmis aux cellules filles ou même aux enfants pendant la reproduction.
- L'épigénétique peut influencer indépendamment des traits non codés par l'ADN, tels que le comportement, la sensibilité aux maladies et le vieillissement.
- L'expression génique fait référence à la fréquence ou au moment où les protéines sont créées à partir des instructions contenues dans les gènes.
- La transcription peut être activée ou désactivée en fonction de différents facteurs, permettant au corps de s'adapter à différentes situations.
- Le cancer implique des milliers de mutations dans le génome et l'épigénome.
- La prédisposition génétique n'est qu'un aspect du cancer.
- L'expression des gènes, influencée par le régime alimentaire et l'environnement, peut activer la prédisposition génétique au cancer.
- Les changements épigénétiques peuvent affecter le risque de développer un cancer et de répondre au traitement.
- La forte incidence du cancer dans les sociétés occidentales avec un régime américain standard est due à l'expression des gènes plutôt qu'aux mauvais gènes.
- La méthylation de l'ADN bloque l'accès aux gènes, désactive les gènes et désactive le système immunitaire.
- La méthylation peut augmenter le risque de cancer et rendre le cancer plus agressif.
- La modification des histones peut affecter les gènes qui régulent le cycle cellulaire, l'apoptose ou l'angiogenèse.
- Des mutations dans divers gènes augmentent le risque de cancer, mais une régulation supplémentaire par la méthylation, la modification des histones ou l'ARN non codant peut encore augmenter le risque ou rendre le cancer plus difficile à traiter.
- Les antioxydants peuvent empêcher ou inverser la méthylation de l'ADN causée par les radicaux libres ou les toxines.
- Les antioxydants peuvent moduler les modifications des histones en influençant les enzymes et en modifiant la structure de la chromatine.
- Les antioxydants peuvent réguler l'ARN non codant, modifiant la régulation des gènes.
- Les antioxydants peuvent prévenir ou réparer les dommages à l'ADN et restaurer l'expression normale des gènes, ralentissant ainsi le développement du cancer.
- Le folate fournit des groupes méthyle pour la méthylation de l'ADN.
- Une carence en folate peut altérer la méthylation de l'ADN et provoquer une expression génique anormale.
- Une carence en folate peut altérer la fonction cognitive et augmenter le risque de démence.
- L'acide folique n'est pas le même que le folate.
- La restriction calorique ralentit le vieillissement et module l'inflammation, le stress oxydatif, le métabolisme et les voies d'autophagie.
- La restriction calorique augmente l'expression des gènes qui protègent contre les dommages cellulaires et la mort.
- La restriction calorique était une partie normale de notre évolution en raison de la rareté.
- Notre corps réagit à la restriction en se réparant et en ralentissant le métabolisme.
- Un régime alimentaire complet à base de plantes induit naturellement une restriction calorique tout en répondant aux besoins nutritionnels.
- Le régime américain standard (SAD) entraîne un excès de calories et un risque accru de maladie en raison de l'huile, du sucre et de aliments très appétissants.
- Les fibres affectent le microbiote intestinal en stimulant les bactéries probiotiques et en régulant négativement le nombre de bactéries carnivores non probiotiques.
- Les métabolites produits par le microbiote intestinal peuvent affecter les organes et les tissus et les fibres peuvent affecter le type et la quantité de ces métabolites.
- Les fibres peuvent moduler la régulation épigénétique et modifier l'expression des gènes impliqués dans l'inflammation, l'immunité et le métabolisme.
- Les fibres peuvent protéger contre l'obésité et le diabète en modulant l'expression des gènes impliqués dans l'homéostasie du glucose, le métabolisme des lipides et la dépense énergétique.
- Les fibres peuvent améliorer la fonction immunitaire en modulant l'expression des gènes impliqués dans l'inflammation, l'immunité et la fonction de barrière et en régulant à la baisse le nombre de bactéries non probiotiques.
- Les fibres peuvent stimuler la production d'anticorps et de cytokines pour combattre les germes.
- Plus de fibres, c'est généralement mieux.
- Trop de fibres peuvent provoquer des ballonnements, des gaz et une augmentation des selles.
- De nombreux facteurs peuvent provoquer des changements épigénétiques, tels que le tabagisme, l'exercice, le stress, les drogues, la pollution ou les traumatismes.
- Vos gènes ne sont pas fixes et peuvent être modifiés par vos choix.
- Une alimentation riche en antioxydants et en fibres est recommandée tout en évitant les bioaccumulation de mutagènes et de toxines dans une chaîne alimentaire.
- Les régimes trop caloriques et pauvres en nutriments doivent être évités, et une restriction calorique avec jeûne intermittent est recommandée.
- Un apport excessif en protéines peut surexprimer l'IGF1 et augmenter le risque de cancer.
FAQ
Références :
- Peixoto, P., Cartron, PF, Serandour, AA, & Hervouet, E. (2020). De 1957 à nos jours : une brève histoire de l'épigénétique. Revue internationale des sciences moléculaires, 21(20), 7571. https://doi.org/10.3390/ijms21207571
- Qu'est-ce que l'épigénétique ? | CDC. (2022, 15 août). Centres pour le Contrôle et la Prévention des catastrophes. https://www.cdc.gov/genomics/disease/epigenetics.htm
- LaPelusa, A., & Kaushik, R. (2022). Physiologie, Protéines. Dans StatPearls. Édition StatPearls. [PubMed]
- Blackwell, TK et Walker, AK (2006). Mécanismes de transcription. WormBook : la revue en ligne de la biologie de C. elegans, 1–16. https://doi.org/10.1895/wormbook.1.121.1
- Hamilton JP (2011). L'épigénétique : principes et pratique. Maladies digestives (Bâle, Suisse), 29(2), 130–135. https://doi.org/10.1159/000323874
- Fanucchi, S., Dominguez-Andres, J., Joosten, LAB, Netea, MG, & Mhlanga, MM (2021). L'intersection de l'épigénétique et du métabolisme dans l'immunité entraînée. Immunité, 54(1), 32–43. https://doi.org/10.1016/j.immuni.2020.10.011
- Surace, AEA et Hedrich, CM (2019). Le rôle de l'épigénétique dans les maladies auto-immunes/inflammatoires. Frontières en immunologie, 10, 1525. https://doi.org/10.3389/fimmu.2019.01525
- Denhardt, DT (2018). Effet du stress sur la biologie humaine : épigénétique, adaptation, hérédité et signification sociale. Journal de physiologie cellulaire, 233(3), 1975-1984. https://doi.org/10.1002/jcp.25837
- de Magalhães-Barbosa, MC, Prata-Barbosa, A., & da Cunha, AJLA (2022). Stress toxique, épigénétique et développement de l'enfant. revue de pédiatrie, 98 Supplément 1(Suppl 1), S13–S18. https://doi.org/10.1016/j.jped.2021.09.007
- Cavalli, G., & Heard, E. (2019). Les progrès de l'épigénétique relient la génétique à l'environnement et à la maladie. Nature, 571(7766), 489–499. https://doi.org/10.1038/s41586-019-1411-0
- Brena, RM, & Costello, JF (2007). Interactions génome-épigénome dans le cancer. Génétique moléculaire humaine, 16 Spec No 1, R96–R105. https://doi.org/10.1093/hmg/ddm073
- Shen, H., & Laird, PW (2013). Interaction entre le génome du cancer et l'épigénome. Cellule, 153(1), 38–55. https://doi.org/10.1016/j.cell.2013.03.008
- Hullar, MA, et Fu, C.-B. (2014). Alimentation, microbiote intestinal et épigénétique. Journal du cancer (Sudbury, Mass.), 20(3), 170–175. https://doi.org/10.1097/PPO.0000000000000053
- Abdul, QA, Yu, BP, Chung, HY, Jung, HA et Choi, JS (2017). Modifications épigénétiques de l'expression des gènes par le mode de vie et l'environnement. Archives de la recherche pharmaceutique, 40(11), 1219-1237. https://doi.org/10.1007/s12272-017-0973-3
- Catteau, A., & Morris, JS (2002). Méthylation de BRCA1 : un rôle significatif dans le développement tumoral ? Séminaires en Biologie du Cancer, 12(5), 359–371. https://doi.org/10.1016/s1044-579x(02)00056-1
- Prajzendanc, K., Domagała, P., Hybiak, J., Ryś, J., Huzarski, T., Szwiec, M., Tomiczek-Szwiec, J., Redelbach, W., Sejda, A., Gronwald, J ., Kluz, T., Wiśniowski, R., Cybulski, C., Łukomska, A., Białkowska, K., Sukiennicki, G., Kulczycka, K., Narod, SA, Wojdacz, TK, Lubiński, J., … Jakubowska, A. (2020). La méthylation du promoteur BRCA1 dans le sang périphérique est associée au risque de cancer du sein triple négatif. Journal international du cancer, 146(5), 1293-1298. https://doi.org/10.1002/ijc.32655
- Yue, X., Zhao, Y., Xu, Y., Zheng, M., Feng, Z. et Hu, W. (2017). Mutant p53 dans le cancer : accumulation, gain de fonction et thérapie. Journal de biologie moléculaire, 429(11), 1595-1606. https://doi.org/10.1016/j.jmb.2017.03.030
- Saliani, M., Jalal, R. et Javadmanesh, A. (2022). Analyse de l'expression différentielle des gènes et des ARN longs non codants associés à la mutation KRAS dans les cellules cancéreuses colorectales. Rapports scientifiques, 12(1), 7965. https://doi.org/10.1038/s41598-022-11697-5
- Beetch, M., Harandi-Zadeh, S., Shen, K., Lubecka, K., Kitts, D. D., O'Hagan, H. M. et Stefanska, B. (2020). Les antioxydants alimentaires remodèlent les schémas de méthylation de l'ADN dans les maladies chroniques. Revue britannique de pharmacologie, 177(6), 1382-1408. https://doi.org/10.1111/bph.14888
- Crider, K. S., Yang, T. P., Berry, R. J. et Bailey, L. B. (2012). Folate and DNA methylation : a review of molecular mechanisms and the evidence for folate's role (Folate et méthylation de l'ADN : une revue des mécanismes moléculaires et des preuves du rôle du folate). Les progrès de la nutrition (Bethesda, Md.), 3(1), 21–38. https://doi.org/10.3945/an.111.000992
- Gensous, N., Franceschi, C., Santoro, A., Milazzo, M., Garagnani, P. et Bacalini, MG (2019). L'impact de la restriction calorique sur les signatures épigénétiques du vieillissement. Revue internationale des sciences moléculaires, 20(8), 2022. https://doi.org/10.3390/ijms20082022
- Choi, SW, & Friso, S. (2010). L'épigénétique : un nouveau pont entre nutrition et santé. Les progrès de la nutrition (Bethesda, Md.), 1(1), 8–16. https://doi.org/10.3945/an.110.1004
- Borzabadi, S., Oryan, S., Eidi, A., Aghadavod, E., Daneshvar Kakhaki, R., Tamtaji, O. R., Taghizadeh, M., & Asemi, Z. (2018). Les effets de la supplémentation en probiotiques sur l'expression des gènes liés à l'inflammation, à l'insuline et aux lipides chez les patients atteints de la maladie de Parkinson : Un essai randomisé, en double aveugle, contrôlé par placebo. Archives de la médecine iranienne, 21(7), 289–295. [PubMed]
- Ye, J., Wu, W., Li, Y. et Li, L. (2017). Influences du microbiote intestinal sur la méthylation de l'ADN et la modification des histones. Maladies et sciences digestives, 62(5), 1155-1164. https://doi.org/10.1007/s10620-017-4538-6
- Bhattacharjee, S., & Dashwood, RH (2020). Régulation épigénétique de NRF2/KEAP1 par des substances phytochimiques. Antioxydants (Bâle, Suisse), 9(9), 865. https://doi.org/10.3390/antiox9090865
- Griñan-Ferré, Christian. et coll. "Antioxydants alimentaires, épigénétique et vieillissement cérébral : focus sur le resvératrol." Stress oxydatif et antioxydants alimentaires dans les maladies neurologiques, édité par Colin R. Martin et Victor R. Preedy, Academic Press, 2020, pp. 343-57 https://doi.org/10.1016/B978-0-12-817780-8.00022-0
- Chhabria, SV, Akbarsha, MA, Li, AP, Kharkar, PS et Desai, KB (2015). Génération d'allicine in situ à l'aide d'une administration ciblée d'alliinase pour l'inhibition des cellules MIA PaCa-2 via des modifications épigénétiques, le stress oxydatif et l'expression de l'inhibiteur de la kinase dépendante de la cycline (CDKI). Apoptose : une revue internationale sur la mort cellulaire programmée, 20(10), 1388-1409. https://doi.org/10.1007/s10495-015-1159-4
- Crider, K. S., Yang, T. P., Berry, R. J. et Bailey, L. B. (2012). Folate and DNA methylation : a review of molecular mechanisms and the evidence for folate's role (Folate et méthylation de l'ADN : une revue des mécanismes moléculaires et des preuves du rôle du folate). Les progrès de la nutrition (Bethesda, Md.), 3(1), 21–38. https://doi.org/10.3945/an.111.000992
- En ligneSaitsu, H. (2017). Récepteurs de folate et fermeture du tube neural. Anomalies congénitales, 57(5), 130–133. https://doi.org/10.1111/cga.12218
- Abraham, KJ, Ostrowski, LA et Mekhail, K. (2017). Les molécules d'ARN non codantes relient la restriction calorique et la durée de vie. Journal de biologie moléculaire, 429(21), 3196–3214. https://doi.org/10.1016/j.jmb.2016.08.020
- Patel, SA, Velingkaar, N., Macwana, K., Chaudhari, A. et Kondratov, R. (2016). La restriction calorique régule l'expression des gènes de l'horloge circadienne par des mécanismes dépendants et indépendants de BMAL1. Rapports scientifiques, 6, 25970. https://doi.org/10.1038/srep25970
- Gabandé-Rodríguez, E., Gómez de Las Heras, MM, & Mittelbrunn, M. (2019). Contrôle de l'inflammation par les mimétiques de restriction calorique : au carrefour de l'autophagie et des mitochondries. Cellules, 9(1), 82. https://doi.org/10.3390/cells9010082
- Bagherniya, M., Butler, AE, Barreto, GE et Sahebkar, A. (2018). L'effet du jeûne ou de la restriction calorique sur l'induction de l'autophagie : une revue de la littérature. Revues de recherche sur le vieillissement, 47, 183–197. https://doi.org/10.1016/j.arr.2018.08.004
- Komatsu, T., Park, S., Hayashi, H., Mori, R., Yamaza, H. et Shimokawa, I. (2019). Mécanismes de la restriction calorique : examen des gènes requis pour les effets de la restriction calorique sur la prolongation de la vie et l'inhibition des tumeurs. Nutriments, 11(12), 3068. https://doi.org/10.3390/nu11123068
- En ligneGreger M. (2020). Un régime alimentaire complet à base de plantes est efficace pour perdre du poids : les preuves. Revue américaine de médecine du style de vie, 14(5), 500–510. https://doi.org/10.1177/1559827620912400
- Makki, K., Deehan, EC, Walter, J. et Bäckhed, F. (2018). L'impact des fibres alimentaires sur le microbiote intestinal dans la santé et la maladie de l'hôte. Hôte cellulaire et microbe, 23(6), 705–715. https://doi.org/10.1016/j.chom.2018.05.012
Articles Similaires
Vous avez des questions sur la nutrition et la santé ?
J'aimerais avoir de vos nouvelles et y répondre dans mon prochain post. J'apprécie votre contribution et votre opinion et j'ai hâte d'avoir de vos nouvelles bientôt. Je vous invite également à nous suivre sur Facebook, Instagram et Pinterest pour plus de contenu sur l'alimentation, la nutrition et la santé. Vous pouvez y laisser un commentaire et entrer en contact avec d'autres passionnés de santé, partager vos conseils et expériences, et obtenir le soutien et les encouragements de notre équipe et de notre communauté.
J'espère que ce billet a été instructif et agréable pour vous et que vous êtes prêt à mettre en pratique les connaissances que vous avez acquises. Si vous avez trouvé ce billet utile, veuillez le partager à vos amis et à votre famille qui pourraient également en bénéficier. On ne sait jamais qui peut avoir besoin de conseils et de soutien dans son parcours de santé.
– Vous pourriez aussi aimer –

Apprendre la Nutrition
Milos Pokimica est docteur en médecine naturelle, nutritionniste clinique, rédacteur en santé médicale et nutrition et conseiller en sciences nutritionnelles. Auteur de la série de livres Devenir vegetarien ? Examen des sciences, il exploite également le site Web de santé naturelle GoVeganWay.com
Avis de non-responsabilité médicale
GoVeganWay.com vous propose des critiques des dernières recherches liées à la nutrition et à la santé. Les informations fournies représentent l'opinion personnelle de l'auteur et ne sont pas destinées ni implicitement à remplacer un avis médical professionnel, un diagnostic ou un traitement. Les informations fournies sont fournies à titre informatif uniquement et ne sont pas destinées à remplacer la consultation, le diagnostic et/ou le traitement médical d'un médecin ou d'un prestataire de soins de santé qualifié.NE JAMAIS IGNORER LES CONSEILS MÉDICAUX PROFESSIONNELS OU RETARDER LA RECHERCHE DE SOINS MÉDICAUX EN RAISON DE QUELQUE CHOSE QUE VOUS AVEZ LU OU ACCÉDÉ SUR GoVeganWay.com
N'APPLIQUEZ JAMAIS DE CHANGEMENTS AU STYLE DE VIE OU TOUT CHANGEMENT À LA SUITE DE QUELQUE CHOSE QUE VOUS AVEZ LU SUR GoVeganWay.com AVANT DE CONSULTER UN PRATICIEN MÉDICAL AGRÉÉ.
En cas d'urgence médicale, appelez immédiatement un médecin ou le 911. GoVeganWay.com ne recommande ni n'approuve aucun groupe, organisation, test, médecin, produit, procédure, opinion ou autre information spécifique pouvant être mentionné à l'intérieur.
Choix de l'éditeur -
Milos Pokimica est rédacteur spécialisé dans la santé et la nutrition et conseiller en sciences nutritionnelles. Auteur d'une série de livres Devenir vegetarien ? Examen des sciences, il exploite également le site Web de santé naturelle GoVeganWay.com
Derniers articles –
Top Des Nouvelles Sur la Santé - ScienceDaily
- Scientists say NAD+ could slow aging and fight Alzheimer’s and Parkinson’sle mars 24, 2026
A global team of leading scientists is zeroing in on a tiny but powerful molecule that could reshape how we age. Known as NAD⁺, it plays a crucial role in keeping our cells energized, repairing DNA, and maintaining overall health—but its levels steadily decline over time, potentially fueling diseases like Alzheimer’s and Parkinson’s. Researchers are now exploring ways to boost NAD⁺ using compounds like NR and NMN, with early studies hinting at improvements in memory, metabolism, and […]
- Insulin pills may soon replace daily injectionsle mars 24, 2026
For over a century, scientists have chased the dream of insulin pills, but the digestive system kept destroying the drug before it could work—forcing millions of patients to rely on daily injections. Now, researchers at Kumamoto University have developed a clever workaround using a tiny peptide that helps insulin slip through the intestinal wall.
- Scientists discover hormone that may stop chronic back pain at its sourcele mars 24, 2026
A new study suggests a widely used bone hormone could help relieve chronic back pain in an unexpected way. Instead of just strengthening bone, it appears to stop pain-sensing nerves from growing into damaged spinal areas. In animal models, this led to stronger spinal tissue and reduced pain sensitivity. The findings hint at a future treatment that tackles back pain at its biological roots.
- Women over 50 lost 35% more weight with this surprising combole mars 24, 2026
Postmenopausal women may have a powerful new edge in the battle against weight gain. A Mayo Clinic study found that those using menopausal hormone therapy while taking the obesity drug tirzepatide lost about 35% more weight than those on the drug alone. The findings hint at a surprising synergy between hormones and cutting-edge weight-loss medications, potentially opening the door to more effective, personalized treatments for millions of women facing increased cardiometabolic risks after […]
- This new tooth powder whitens teeth without damagele mars 24, 2026
Researchers have developed a teeth-whitening powder that works with the vibrations of an electric toothbrush to safely remove stains. Unlike traditional whiteners, it not only brightens teeth but also repairs enamel and supports healthy oral bacteria. Lab tests showed dramatic whitening effects, while animal studies revealed reduced harmful microbes and inflammation. This could pave the way for a new generation of at-home dental care.
- Scientists discover Alzheimer’s hidden “death switch” in the brainle mars 23, 2026
Scientists have uncovered a hidden “death switch” in the brain that may be driving Alzheimer’s disease—and even found a way to turn it off in mice. The culprit is a toxic pairing of two proteins that, when combined, triggers the destruction of brain cells and fuels memory loss. By using a new compound to break apart this deadly duo, researchers were able to slow disease progression, protect brain cells, and even reduce hallmark amyloid buildup.
- New blood test could catch pancreatic cancer before it’s too latele mars 23, 2026
A new blood test could change the outlook for one of the deadliest cancers—pancreatic cancer—by catching it much earlier than ever before. Researchers identified two previously unknown proteins in the blood that, when combined with existing markers, dramatically improved detection accuracy. The four-marker test was able to spot pancreatic cancer in over 90% of cases and performed especially well even in early stages, when treatment has the best chance of success.
PubMed, #régime-vegan –
- Plant-Based Dietary Patterns and Neuroimaging Biomarkers of Brain Health: A Scoping Review of Observational and Interventional Evidencele mars 23, 2026
Healthy dietary interventions are well established in cardiovascular disease prevention, but their effects on the brain remain underexplored. This scoping review aims to investigate how adherence to core components of a whole-food plant-based diet (WFPBD) may impact neuroimaging outcomes across different brain conditions. We searched PubMed and MEDLINE for studies published in the past 20 years evaluating the effects of a predominantly or exclusively WFPBD, alone or combined with other […]
- Environmental and economic impact of a vegan versus traditional mediterranean diet: OMNIVEG studyle mars 17, 2026
CONCLUSIONS: Replacing animal products with plant-based foods in a Mediterranean dietary framework can enhance environmental sustainability and reduce food costs. These findings support the promotion of whole plant-based diets as a viable strategy for sustainable and affordable nutrition.
- Consumption Habits and Perception of Plant-Based Milk and Dairy Alternatives Among Vegetarians and Omnivores: A Case Study of Consumers in Sloveniale mars 14, 2026
CONCLUSIONS: PBMDA perceptions in Slovenia are strongly segmented by dietary pattern and socio-demographics, supporting the need for clearer nutrition communication.
- Culinary Nutrition Programming for Members of a Community-Based Cancer Programle mars 14, 2026
(1) Background: Nutrition research in cancer care has largely focused on disease prevention and management, overlooking the importance of food literacy. Culinary cancer care programs may address this gap by facilitating the practical application of nutrition through culinary skills, fostering social connections over nutrient-dense meals, and supporting individuals during periods of physical and social vulnerability. The Not-Just-Supper Club (NJSC) at Gilda’s Club Toronto (GT) is a…
- Fatty acid composition of ground-beef products and their plant-based meat substitutes available in Hungaryle mars 13, 2026
CONCLUSION: The findings indicate that plant-based meat alternatives (except those containing coconut oil) have lower saturated and higher polyunsaturated fatty acid compositions than beef-based products, leading to more beneficial nutritional value. Further analytical and clinical studies are necessary to provide a more comprehensive understanding of the long-term health effects of these foods.
Messages aléatoires –
Postes en vedette -
Dernières Nouvelles de PubMed, #alimentation végétale –
- Comment on “Plant-based diet and risk of arthritis: a nationwide cohort study of the Chinese elderly population” by H. Zhang, J. Liang, Y. Han, J. Tian, Y. Tu, R. Fan, W. Zhu, Z. Zhang and H. Zhao,…par Tong Xin le mars 24, 2026
A stratified perspective is essential to understand the divergent impacts of plant-based diets on osteoarthritis risk in older populations.
- A Mediterranean lifestyle obesity prevention intervention in preschoolers at risk: MELI-POP Study-a randomized controlled trialpar A Larruy-García le mars 24, 2026
CONCLUSION: A Mediterranean lifestyle intervention may benefit body composition changes in preschool girls at risk of obesity; larger studies are needed to confirm these sex-specific results.
- From cow to crop: motives and barriers for plant-based dairy alternative consumption across three European countriespar Dominika Maison le mars 23, 2026
Currently, alternative sources of protein are being sought to replace not only meat but also dairy products in the diet. From this perspective, it is worth examining how consumers perceive these products, what motivates them to choose them and what barriers they encounter, especially with regard to attitudes towards dairy products. The present study aimed to compare attitudes towards plant-based dairy alternatives (PBDAs) in three European countries – Poland, Germany and the UK. Furthermore, […]
- Energy and macronutrient intakes of Montenegrin adults: insights from the EFSA EU Menu National Survey (2017-2022)par Amil Orahovac le mars 23, 2026
INTRODUCTION: Understanding population-level dietary intakes is essential for preventing diet-related non-communicable diseases (NCDs) and informing evidence-based nutrition policies. Until recently, Montenegro lacked nationally representative data on food and nutrient intake aligned with European Food Safety Authority (EFSA) standards. This study provides the first comprehensive analysis of energy and macronutrient intake among Montenegrin adults within the EFSA EU Menu framework.
- Plant-Based Dietary Patterns and Neuroimaging Biomarkers of Brain Health: A Scoping Review of Observational and Interventional Evidencepar Lydia Viviana Falsitta le mars 23, 2026
Healthy dietary interventions are well established in cardiovascular disease prevention, but their effects on the brain remain underexplored. This scoping review aims to investigate how adherence to core components of a whole-food plant-based diet (WFPBD) may impact neuroimaging outcomes across different brain conditions. We searched PubMed and MEDLINE for studies published in the past 20 years evaluating the effects of a predominantly or exclusively WFPBD, alone or combined with other […]
- Metabolic pathway analysis reveals hierarchical pentose sugar utilization and metabolic flexibility of Bifidobacterium longumpar Lisa Friess le mars 23, 2026
Plant-derived pentose sugars represent a major nutrient source in the gut, yet their metabolism remains incompletely defined. Strains of the human gut commensal Bifidobacterium longum subsp. longum utilise arabinose- and xylose-containing glycans, which are found in the pectin and hemicellulose layers of plant cell walls. To gain insight into the metabolism of these two pentoses as well as ribose, a naturally occurring sugar and a component of RNA and ATP, we identified and analysed the genes…