Le lait A1 avec la variante bêta-caséine a1 est un facteur de risque possible dans le développement du diabète de type 1 chez les enfants, de l'autisme et des maladies cardiaques chez les adultes.
Milos Pokimica
Écrit par : Milos Pokimica
Examiné Médicalement Par : Dr. Xiùying Wáng, M.D.
Mis à jour le 10 juin 2023Principaux Enseignements :
- La bêta-caséine est une protéine qui représente environ 30% des protéines du lait de vache. Elle existe sous deux variantes génétiques : A1 et A2.
- La bêta-caséine A1 du lait de vache est différente de celle de tous les autres mammifères, qui sont exclusivement de type A2, y compris les bovins A2 d'Inde et d'Afrique, les buffles, ainsi que les autres mammifères et le lait humain. Presque tous les bovins de type A1 sont apparentés aux vaches d'origine européenne de la sous-espèce d'origine de cette mutation, Bos Taurus.
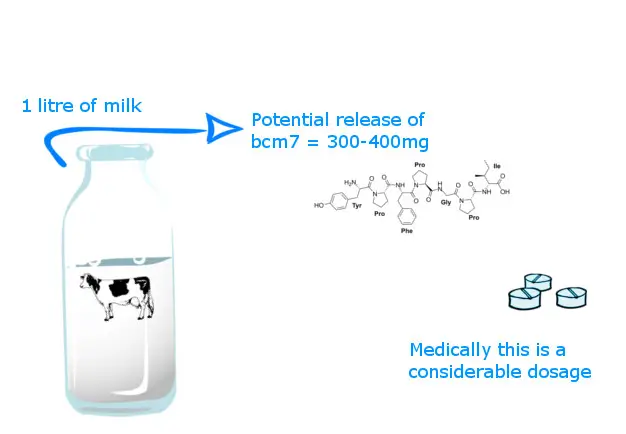
- Le BCM7 est un peptide qui se décompose en 7 acides aminés à partir de la bêta-caséine A1. Il a des effets opiacés similaires à ceux des narcotiques tels que la morphine et peut être nocif pour les lipoprotéines de basse densité (LDL).
- Il existe une corrélation entre le diabète de type 1 et les anticorps dirigés contre la bêta-caséine A1. On pense que ces anticorps attaquent les cellules qui produisent l'insuline dans le pancréas en raison de similitudes avec la structure de la protéine BCM7.
- Les casomorphines sont des opioïdes que l'on trouve dans les produits laitiers, en particulier dans la bêta-caséine A1. Elles ont été associées à l'autisme et à la schizophrénie dans le cadre de la théorie de "l'excès d'opioïdes".
- Les peptides opioïdes du lait de vache ont longtemps été considérés comme une cause possible du syndrome de mort subite du nourrisson (SMSN), car ils peuvent inhiber le centre respiratoire du tronc cérébral, entraînant l'apnée et la mort.
- Des irBCM (casomorphines bovines) basales élevées ont été observées chez les nourrissons nourris au lait maternisé présentant un retard dans le développement psychomoteur et un tonus musculaire accru, tandis que les irHCM (casomorphines humaines) basales les plus élevées ont été observées chez les nourrissons nourris au lait maternel présentant un développement psychomoteur et un tonus musculaire normaux.
Bêta-caséine A1 dans le lait de vache.
La bêta-caséine représente environ 30% de la protéine du lait de vache. La bêta-caséine est présente sous la forme d'une ou deux variantes génétiques : A1 ou A2. La plupart du lait de vache contient une combinaison de bêta-caséine A1 et A2. Toutefois, il existe dans certains pays du lait qui ne contient que le type A2, sans bêta-caséine A1 alpha.
La deuxième variante, la bêta-caséine A2, n'est pas associée au diabète de type 1.
La relation établie entre la béta-caséine A1 et le diabète de type 1 et les maladies cardiaques est de 0,982 et 0,76 (Laugesen et Elliott, 2003).
Il s'agit d'un niveau très significatif si on le compare à d'autres raisons épidémiologiques de ces conditions, telles que le tabagisme et la mortalité par cancer du poumon r = 0,73 ou la probabilité de personnes dans les années 1960 et de maladies cardiaques dix ans plus tard où r = 0,85.
La différence entre la bêta-caséine A1 et A2 est présente en raison d'une seule substitution d'acides aminés à 67 lignes d'acides aminés de 209 qu'ils ont dans la chaîne.
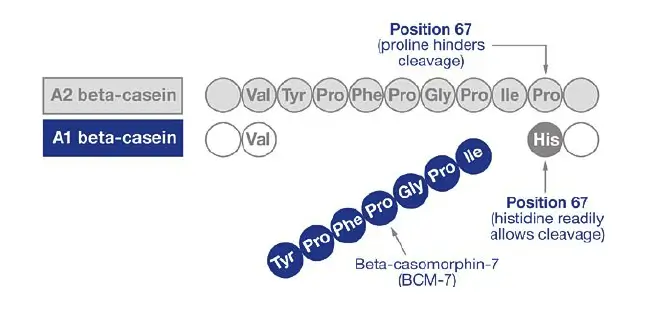
La bêta-caséine A1 du lait de vache est différente de celle de tous les autres mammifères, qui sont exclusivement de type A2, y compris les bovins A2 d'Inde et d'Afrique, les buffles, ainsi que les autres mammifères et le lait humain. Presque tous les bovins de type A1 sont apparentés aux vaches d'origine européenne de la sous-espèce d'origine de cette mutation, Bos Taurus.

Elle résulte d'une mutation génétique des vaches en Europe, survenue il y a environ 8 000 ans. Aujourd'hui, les vaches laitières A1 sont élevées en Europe et en Amérique, et les espèces A2 sont élevées en Nouvelle-Zélande. Les vaches de la race Holstein ont des quantités presque égales de bêta-caséine A1 et A2. L'espèce Jersey possède généralement un peu plus de A2, mais elle est également considérée comme une espèce mixte. Les mêmes vaches Jersey sont porteuses d'une bêta-caséine "B" qui s'est avérée donner plus de BCM7. En raison d'une mauvaise fixation de l'histidine, la bêta-caséine A1 se décompose en peptides de 7 acides aminés appelés bêta-casomorphine 7 (BCM7) lorsqu'elle est consommée. La BCM7 est problématique car l'opiacé est au même niveau que les narcotiques comme la morphine et a des effets similaires. Il s'agit également d'un oxydant connu pour ses effets néfastes sur la santé. lipoprotéines de basse densité (LDL). Comme les liens entre les 7 acides aminés le rendent extrêmement solide, il est résistant à toute dégradation ultérieure. Lorsque le BCM7 pénètre dans la circulation sanguine, divers problèmes se posent.
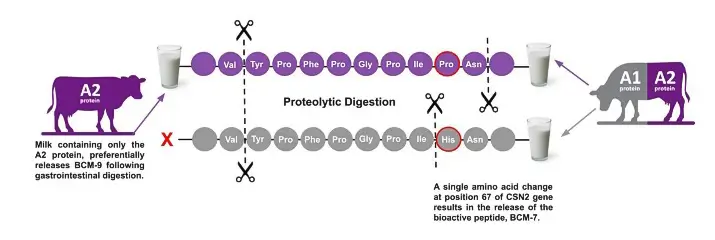
Cependant, le BCM 7 est trop volumineux pour être absorbé par un manteau sain dans l'intestin, ce qui signifie que le problème de santé associé à la bêta-caséine A1 est plus susceptible d'être affecté par des personnes ayant une santé digestive endommagée ou par des maladies telles que maladie coeliaque ou une maladie gastro-intestinale.
Si vous avez un intestin qui fuit, vous pouvez vous donner, à vous et à votre fœtus, si vous êtes enceinte, le diabète de type 1 en tant que maladie auto-immune. si vous consommez du lait et des produits laitiers, c'est-à-dire. Les personnes ayant l'une des conditions en vigueur sont plus appropriées pour l'abcès BCM7. Chez les bébés qui ont naturellement une perméabilité intestinale accrue afin d'améliorer l'absorption des nutriments, le risque est également plus élevé.
Une fois qu'il pénètre dans la circulation sanguine, le BCM7 peut facilement franchir la barrière hémato-encéphalique et pénétrer dans le cerveau, où la connexion aux récepteurs provoque les symptômes de l'autisme et de la schizophrénie.
Cette affirmation a été initiée par des recherches qui ont été diffusées sur des rats, où les rats ont montré des tendances similaires dans le comportement et la sympathie comme l'autisme et la schizophrénie après l'injection de BCM7. L'association de ces effets a également été confirmée par la capacité d'inverser l'état et les modifications du comportement de la naloxone antagoniste des opioïdes. Pour ajouter à cela, il est reconnu depuis longtemps que les opiacés ont un effet sur la fonction immunitaire, qui est la raison possible pour laquelle la bêta-caséine A1 et le BCM7 sont associés à des maladies auto-immunes.
Cardiopathie.
La première découverte a été faite par Alexandra Steinerovath qui a étudié les causes du stress oxydatif chez les nourrissons. Elle a découvert que les bébés nourris au lait maternisé présentaient un taux plus élevé d'anticorps contre les LDL oxydées (Steinerova et al, 1999). En 2004, Steinerova a lancé l'idée et réalisé une étude sur le BCM7 et l'augmentation des anticorps chez les nourrissons. Une étude a démontré que les nourrissons nourris avec des préparations pour bébés à base de bêta-caséine A1 développaient des niveaux significativement plus élevés de ces anticorps par rapport à ceux nourris avec de la bêta-caséine A2 (Steinerova et al., 2004).
Aujourd'hui, plus de recherches ont été effectuées et la communauté scientifique s'attend à ce que le BCM7 ait un effet pro-oxydant sur les LDL. Dans le cas des maladies cardiaques, des études supplémentaires ont permis de découvrir le mécanisme par lequel la bêta-caséine A1 va développer la maladie cardiaque. maladie cardiaque, et l'effet principal est un BCM7 qui oxyde le LDL qui transporte le cholestérol du foie vers les tissus (Chin-Dusting et al., 2006). Ceci est important car les LDL oxydées augmentent le risque de maladie cardiaque en raison de l'augmentation de l'incidence des artères et, par conséquent, de l'accumulation de la plaque, c'est-à-dire que les LDL oxydées rendent les artères collantes et conduisent à la formation de la plaque.
Diabète de type 1.
Le diabète de type 1 est classé comme un maladie auto-immune qui se produit en raison d'un assaut du système immunitaire sur les cellules qui produisent l'insuline dans le pancréas.
Et ce n'est pas génétique comme on pourrait le faire croire par la médecine conventionnelle. La prédisposition génétique joue un rôle, mais pour prouver qu'il ne s'agit que d'une maladaptation de plus, nous pouvons regarder des jumeaux identiques. La concordance du diabète de type 1 chez les vrais jumeaux n'est que de 50 %. Cela signifie que l'on comprend, on ne comprend pas. Si c'est génétique et que l'environnement ne joue pas un rôle, cela ne se produirait pas. C'est quelque chose que nous avons mangé ou pour être précis que les mères ont mangé ou donné aux bébés qui les amènent à développer cette maladie auto-immune.
Au Japon, le taux de diabète de type 1 est 18 fois moins élevé qu'aux États-Unis, mais lorsque les Japonais émigrent en Amérique et commencent à adopter le régime alimentaire occidental, ils développent le même taux de diabète que les Américains. Certains pays ont 100 fois moins de taux de diabète de type 1 que d'autres, en fonction principalement du régime alimentaire de la population. Le diabète de type 1 a commencé à augmenter après la Seconde Guerre mondiale, comme d'autres maladies, il n'est donc pas génétique. C'est une mauvaise adaptation, et nous savons maintenant ce qui en est la cause.
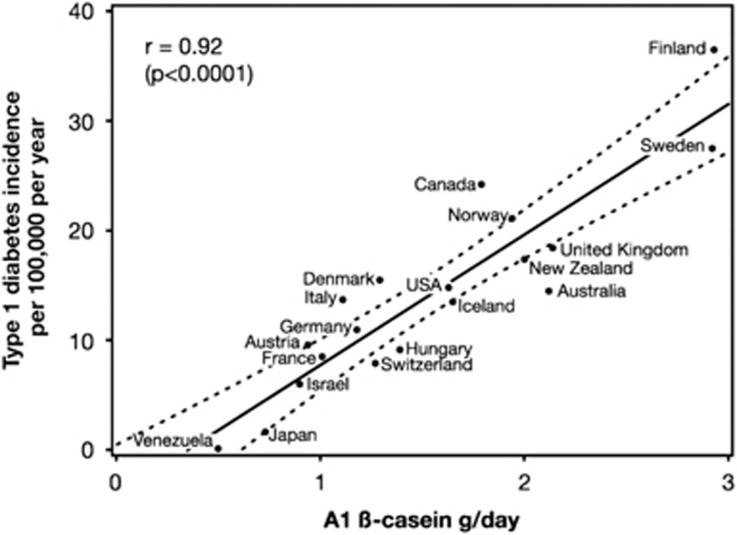
En 1999, les universitaires découvert en Allemagne qu'il existe une corrélation entre le diabète de type 1 et le niveau d'anticorps contre la bêta-caséine A1. On pense que ces anticorps sont, en fait, basés sur la séquence d'acides aminés de l'opioïde problématique BCM7, qui est dérivé de la bêta-caséine A1. Comme la séquence présente des similitudes avec la structure protéique des cellules qui produisent l'insuline dans le pancréas, les anticorps attaquent le pancréas en même temps que les peptides BCM7. Dans cette étude, tous les enfants présentaient des niveaux significatifs d'anticorps anti-bêta-caséine A1 dans leur sang, mais pas d'anticorps contre d'autres protéines du lait (Karjalainen et al., 1992). La conclusion est la suivante :
"Les patients atteints de diabète sucré insulinodépendant présentent une immunité à l'égard de l'albumine du lait de vache, avec des anticorps dirigés contre un peptide d'albumine capable de réagir avec une protéine de surface spécifique des cellules bêta. Ces anticorps pourraient participer au développement du dysfonctionnement des îlots de Langerhans".
Karjalainen et al., 1992

Autisme, Schizophrénie, et Syndrome de mort subite du nourrisson.
De plus, certains opiacés traversent la barrière hémato-encéphalique. Parce que les opiacés BCM7 ne devraient pas être présents du tout et représentent une forme de mutation non naturelle chez les bovins, cela ne devrait pas être une grande surprise dans la relation entre la bêta-caséine A1 et la caséine en général à l'association avec l'autisme également.
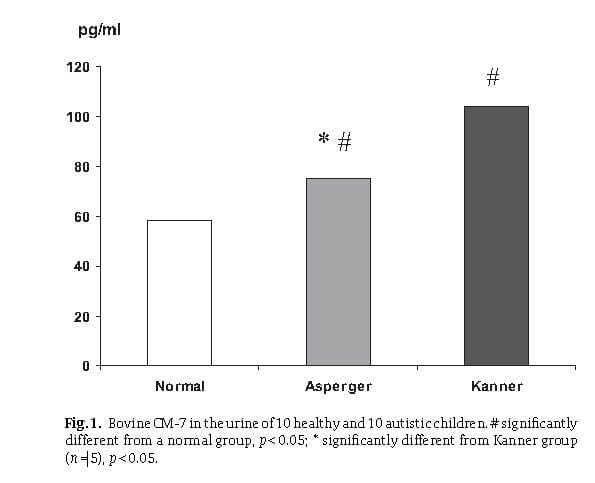
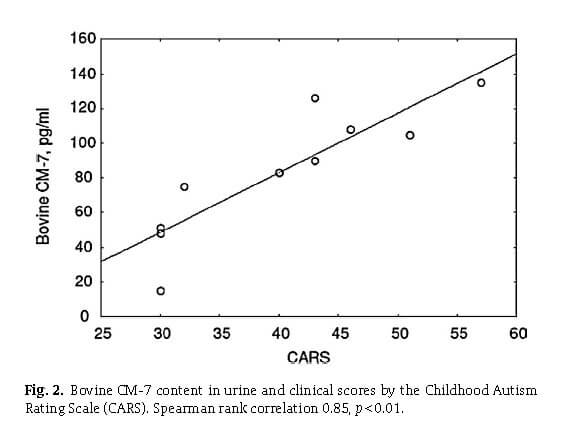
Le BCM 7 obtenu à partir de la bêta-caséine A1 et la glutéomorphine dérivée du gluten sont des opiacés qui peuvent être associés à ces symptômes. À cause de ce, un grand nombre d'enfants autistes montrent des améliorations significatives s'ils évitent le gluten et la caséine. La relation entre l'autisme et les opiacés n'est pas nouvelle. En 1979, Jaak Panksepp, un scientifique, a suggéré ce lien. En 2000, une équipe de chercheurs dirigée par Robert Cade a examiné les preuves existantes liant la caséine et gluten opiacés avec autisme et schizophrénie. Ils ont recueilli de nouvelles données auprès de 150 enfants autistes, 120 adultes schizophrènes, 43 enfants normaux et 76 adultes normaux (Cade et al., 2000). Les enfants autistes et les adultes schizophrènes ont montré une valeur anormale élevée constante des peptides opioïdes casomorphine et glutéomorphine obtenus à partir de la bêta-caséine et du gluten.
En fait, tous les adultes présentent des niveaux élevés de cette substance opioïde morphinique après avoir consommé du lait ou du yaourt, même l'adulte qui ne présente pas d'inflammation dans l'intestin, au moins pendant les 8 heures qui suivent la consommation (Chabance et al., 1998).
La théorie est la suivante : vous avez une prédisposition génétique à des maladies telles que l'autisme ou la schizophrénie. Vous avez une prédisposition génétique à des maladies telles que l'autisme ou la schizophrénie. C'est ce que l'on appelle le "excès d'opioïdesthéorie ".. Vous avez une prédisposition génétique et vous êtes exposé très tôt à des facteurs de stress environnementaux qui endommagent votre intestin et le rendent perméable, ou bien vous êtes un bébé normal qui a naturellement un intestin perméable. Puis vient le lait ou les produits laitiers, avec toutes les casomorphines qui passent en excès dans le sang, puis dans le cerveau, ce qui déclenche l'apparition de la maladie. On pense que ces opioïdes pourraient jouer un rôle dans le développement de l'autisme et d'autres troubles neurologiques. Le problème avec ces casomorphines est aussi que lorsqu'on examine la barrière hémato-encéphalique des patients autistes, leur barrière hémato-encéphalique semble plus faible aussi.
Chez un individu normal, il y aura certains effets sédatifs, mais chez une personne dont l'intestin et la barrière hémato-encéphalique ne sont pas étanches, l'effet sera beaucoup plus fort, et si cette personne a une prédisposition génétique ou une sensibilité à ces substances, alors la véritable maladie peut se développer. Selon la théorie dite de "l'excès d'opioïdes" en tout cas.
Sur les soixante-dix enfants autistes soumis à un régime sans gluten et sans caséine, 81% ont montré des améliorations significatives sur une période de trois mois, et plus d'un tiers de ceux qui ne se sont pas rétablis avaient encore un taux élevé de peptides opioïdes, ce qui indique qu'ils n'ont pas suivi le régime alimentaire de l'enfant. Bien que seuls 40% des adultes aient vu leur état s'améliorer, on pense que nombre d'entre eux n'ont pas suivi le régime suffisamment longtemps pour donner à leur organisme la capacité d'éliminer les molécules BCM7 présentes dans le cerveau, qui peuvent durer plus d'un an.
En 1999, Zhongjie Sun et Robert Cade ont injecté des dérivés opioïdes BCM7 de la bêta-caséine A1 à des rats pour déterminer s'ils pénètrent dans le cerveau (Cade et al., 1999). Ils ont découvert qu'il pénètre dans les différentes zones du cerveau qui ont été précédemment associées à l'autisme et à la schizophrénie. Par conséquent, ils ont pensé que le BCM7 pouvait franchir la barrière hémato-encéphalique et atteindre des parties du cerveau susceptibles d'être affectées par l'autisme et la schizophrénie. La même année, ils ont mené une expérience similaire et ont constaté que les rats auxquels on avait injecté le BCM7 présentaient plusieurs symptômes importants de l'autisme et de la schizophrénie, tels que l'intolérance, une sensibilité réduite à la douleur et l'absence de réaction aux stimuli externes.
En 2003, Sun et Cade ont poursuivi leurs recherches et découvert que les opioïdes gluteomorphin dérivés du gluten n'affectaient que trois régions du cerveau, tandis que les opioïdes BCM7 dérivés de la bêta-caséine A1 affectaient 45 régions. La circulation de ce peptide dans le système nerveux central immature du nourrisson pourrait également inhiber le centre respiratoire du tronc cérébral, ce qui entraînerait l'apnée et la mort (Sun et al, 2003). Les peptides opioïdes du lait ont longtemps été théorisés comme une cause possible de syndrome de mort subite du nourrisson (Ramabadran and Bansinath, 1988).
Cela a non seulement prouvé que BCM7 arrive au cerveau beaucoup plus facilement, mais c'est un facteur beaucoup plus important dans le développement de autisme et schizophrénie. Je ne sais pas si ces études vont permettre de mieux comprendre ou de mieux traiter ces personnes. Il pourrait y avoir des individus ayant une prédisposition génétique à ces maladies que ces protéines de mimétisme moléculaire ne font qu'aggraver. Je n'en sais rien. La science poursuit ses recherches, mais c'est un processus lent et qui aura intérêt à financer ces études ? Cela prendra du temps.
Casomorphines opioïdes et retard psychomoteur.
Le lait A1 contre le lait A2 a eu un gros problème politique en Australie et en Nouvelle-Zélande à un moment donné. Elle s'est terminée par l'étiquetage obligatoire du lait et de tous les produits laitiers. En Australie, vous ne pouvez pas acheter une bouteille de lait A1 ou tout autre produit laitier sans une étiquette visible indiquant si le lait contient une forme de protéine A1 ou A2.

Pourquoi ces opioïdes sont-ils dans le lait en premier lieu ? Et il y en a dans tout le lait existant, pas seulement la variante de lait A1. Le lait A1 est juste une variante plus puissante. Pour les bébés humains normaux ainsi que pour les veaux, ils sont là pour créer une envie ou pour les rendre dépendants comme le sont les toxicomanes réguliers, mais dans ce cas, la dépendance va déclencher la guérison du bébé aux opiacés, puis le bébé va obtenir toute la nutrition du lait dont il a besoin pour grandir. Tout est comme il se doit, mais maintenant nous avons changé d'espèce. Tout comme le profil d'acides aminés protéiques du lait humain et de vache n'est pas le même, le profil de ces casomorphines n'est pas le même.
Dans cette étude (Kost et al., 2009), les bébés nourris avec du lait de vache contenant un taux plus élevé de casomorphines bovines semblent souffrir d'un retard psychomoteur, mais c'est exactement l'inverse qui a été constaté pour les casomorphines humaines. Les casomorphines humaines semblent aider le cerveau des humains. La conclusion de l'étude est la suivante :
" L'irHCM (casomorphines humaines) basal le plus élevé a été observé chez les enfants nourris au sein dont le développement psychomoteur et le tonus musculaire étaient normaux. En revanche, un taux basal élevé d'irBCM (casomorphines bovines) a été observé chez les nourrissons nourris au lait maternisé présentant un retard de développement psychomoteur et un tonus musculaire accru. Chez les nourrissons nourris au lait maternisé dont le développement était normal, le taux de ce paramètre était directement corrélé à l'irBCM basal. Les données indiquent que l'allaitement maternel présente un avantage par rapport à l'alimentation artificielle pour le développement des nourrissons au cours de la première année de vie et soutiennent l'hypothèse de la détérioration de l'élimination de la casomorphine bovine en tant que facteur de risque pour le retard du développement psychomoteur et d'autres maladies telles que l'autisme. "
(Kost et al., 2009)
La structure de la caséine dans le lait humain et dans le lait de vache est sensiblement différente, avec une différence de 47 % seulement, et surtout si nous avons de la caséine A1 mutée dans le mélange, nous avons une situation qui peut déclencher un diabète de type 1 chez le bébé. La casomorphine bovine est beaucoup plus puissante que la casomorphine humaine, et son effet est presque équivalent à celui de la morphine (Trivedi et al., 2015). Les casomorphines de vache se lient plus étroitement aux récepteurs de la sérotonine dans le cerveau que les casomorphines humaines. En outre, les casomorphines opioïdes ont été produites à la fois par le lait A1 et le lait A2, sans différence de puissance (Asledottir et al., 2017). En outre, le lait de vache contient beaucoup plus de caséine en général, 15 fois plus pour être précis que le lait humain. Vingt-et-un peptides et huit provenant de la bêta-caséine ont été trouvés dans le lait de vache, et seulement cinq peptides et un seul provenant de la bêta-caséine ont été trouvés dans le lait humain.

Faut-il passer au A2 qui est dix fois plus cher? Qu'en est-il de la pizza au fromage au lait A1 ou de tout autre produit laitier A1 commercial ? La plupart des chocolats sont fabriqués avec du lait en poudre A1. Le scénario le plus réaliste est que même si nous voulons passer à A2, il n'y a pas de lait A2 si vous vivez en dehors de la Nouvelle-Zélande. Et même en Nouvelle-Zélande, il y a le lait chipset poudre A1 fait pour le industrie alimentaire dans presque tout. De la glace au chocolat. Et même si nous pouvions dépenser de l'argent supplémentaire et avoir cette crème glacée A2, le lait est toujours corrélé, y compris A2, à un large éventail de problèmes de santé (Lait et produits laitiers - Corrélations des risques pour la santé).
Le diable dans le lait, pourquoi ça peut être dangereux.
FAQ
Références :
- Karjalainen, J., Martin, JM, Knip, M., Ilonen, J., Robinson, BH, Savilahti, E., Akerblom, HK et Dosch, HM (1992). Un peptide d'albumine bovine comme déclencheur possible du diabète sucré insulino-dépendant. Le journal de médecine de la Nouvelle-Angleterre, 327(5), 302–307. https://doi.org/10.1056/NEJM199207303270502
- Chabance , B. , Marteau , P. , Rambaud , JC , Migliore-Samour , D. , Boynard , M. , Perrotin , P. , Guillet , R. , Jollès , P. , & Fiat , A. (1998). Libération de peptides de caséine et passage dans le sang chez l'homme lors de la digestion du lait ou du yaourt. Biochimie, 80(2), 155–165. https://doi.org/10.1016/s0300-9084(98)80022-9
- Kost, NV, Sokolov, OY, Kurasova, OB, Dmitriev, AD, Tarakanova, JN, Gabaeva, MV, Zolotarev, YA, Dadayan, AK, Grachev, SA, Korneeva, EV, Mikheeva, IG et Zozulya, AA (2009 ). Bêta-casomorphines-7 chez les nourrissons sous différents types d'alimentation et à différents niveaux de développement psychomoteur. Peptides, 30(10), 1854–1860. https://doi.org/10.1016/j.peptides.2009.06.025
- Trivedi, MS, Hodgson, N., Walker, SG, Trooskens, G., Nair, V. et Deth, RC (2015). Effets épigénétiques des peptides opioïdes dérivés de la caséine dans les cellules de neuroblastome humain SH-SY5Y. Nutrition & Métabolisme, 12(1). https://doi.org/10.1186/s12986-015-0050-1
- Asledottir, T., Le, T. T., Petrat-Melin, B., Devold, T. G., Larsen, L. B., & Vegarud, G. E. (2017). Identification de peptides bioactifs et quantification de la β-casomorphine-7 à partir de la β-caséine bovine A1, A2 et I après digestion gastro-intestinale ex vivo. Journal laitier international, 71, 98-106. https://doi.org/10.1016/j.idairyj.2017.03.008
- Cade, R., Privette, M., Fregly, M., Rowland, N., Sun, Z., Zele, V., Wagemaker, H., & Edelstein, C. (2000). Autisme et schizophrénie : troubles intestinaux. Neurosciences nutritionnelles, 3(1), 57–72. https://doi.org/10.1080/1028415X.2000.11747303
- Pal , S. , Woodford , K. , Kukuljan , S. et Ho , S. (2015). Intolérance au lait, bêta-caséine et lactose. Nutriments, 7(9), 7285-7297. https://doi.org/10.3390/nu7095339
- Chia, JSJ, McRae, JL, Kukuljan, S., Woodford, K., Elliott, RB, Swinburn, B. et Dwyer, KM (2017). Protéine de lait bêta-caséine A1 et autres facteurs environnementaux prédisposant au diabète de type 1. Nutrition & diabète, 7(5), e274. https://doi.org/10.1038/nutd.2017.16
- Sun, Z., Zhang, Z., Wang, X., Cade, R., Elmir, Z. et Fregly, M. (2003). Relation de la bêta-casomorphine à l'apnée dans le syndrome de mort subite du nourrisson. Peptides, 24(6), 937–943. https://doi.org/10.1016/s0196-9781(03)00156-6
- Ramabadran, K., & Bansinath, M. (1988). Les peptides opioïdes du lait comme cause possible du syndrome de mort subite du nourrisson. Hypothèses médicales, 27(3), 181–187. https://doi.org/10.1016/0306-9877(88)90138-7
- Chin-Dusting, J., Shennan, J., Jones, E., Williams, C., Kingwell, B. et Dart, A. (2006). Effet d'une supplémentation alimentaire en bêta-caséine A1 ou A2 sur les marqueurs de développement de la maladie chez les personnes à haut risque de maladie cardiovasculaire. The British journal of nutrition, 95(1), 136–144. https://doi.org/10.1079/bjn20051599
- Steinerová, A., Racek, J., Stozický, F., Tatzber, F., & Lapin, A. (1999). Autoanticorps contre les LDL oxydées dans la première phase de la vie. Lipoprotéines de basse densité. Chimie clinique et médecine de laboratoire, 37(9), 913–917. https://doi.org/10.1515/CCLM.1999.135
- Steinerová, A., Korotvicka, M., Racek, J., Rajdl, D., Trefil, L., Stozický, F. et Rokyta, Z. (2004). Augmentation significative des anticorps dirigés contre les particules de LDL oxydées (IgoxLDL) chez les nourrissons de trois mois ayant reçu du lait maternisé. Athérosclérose, 173(1), 147–148. https://doi.org/10.1016/j.atherosclerosis.2003.12.006
- Laugesen, M., & Elliott, R. (2003). Cardiopathie ischémique, diabète de type 1 et bêta-caséine A1 du lait de vache. La revue médicale néo-zélandaise, 116(1168), U295. [PubMed]
Articles Similaires
Vous avez des questions sur la nutrition et la santé ?
J'aimerais avoir de vos nouvelles et y répondre dans mon prochain post. J'apprécie votre contribution et votre opinion et j'ai hâte d'avoir de vos nouvelles bientôt. Je vous invite également à nous suivre sur Facebook, Instagram et Pinterest pour plus de contenu sur l'alimentation, la nutrition et la santé. Vous pouvez y laisser un commentaire et entrer en contact avec d'autres passionnés de santé, partager vos conseils et expériences, et obtenir le soutien et les encouragements de notre équipe et de notre communauté.
J'espère que ce billet a été instructif et agréable pour vous et que vous êtes prêt à mettre en pratique les connaissances que vous avez acquises. Si vous avez trouvé ce billet utile, veuillez le partager à vos amis et à votre famille qui pourraient également en bénéficier. On ne sait jamais qui peut avoir besoin de conseils et de soutien dans son parcours de santé.
– Vous pourriez aussi aimer –

Apprendre la Nutrition
Milos Pokimica est docteur en médecine naturelle, nutritionniste clinique, rédacteur en santé médicale et nutrition et conseiller en sciences nutritionnelles. Auteur de la série de livres Devenir vegetarien ? Examen des sciences, il exploite également le site Web de santé naturelle GoVeganWay.com
Avis de non-responsabilité médicale
GoVeganWay.com vous propose des critiques des dernières recherches liées à la nutrition et à la santé. Les informations fournies représentent l'opinion personnelle de l'auteur et ne sont pas destinées ni implicitement à remplacer un avis médical professionnel, un diagnostic ou un traitement. Les informations fournies sont fournies à titre informatif uniquement et ne sont pas destinées à remplacer la consultation, le diagnostic et/ou le traitement médical d'un médecin ou d'un prestataire de soins de santé qualifié.NE JAMAIS IGNORER LES CONSEILS MÉDICAUX PROFESSIONNELS OU RETARDER LA RECHERCHE DE SOINS MÉDICAUX EN RAISON DE QUELQUE CHOSE QUE VOUS AVEZ LU OU ACCÉDÉ SUR GoVeganWay.com
N'APPLIQUEZ JAMAIS DE CHANGEMENTS AU STYLE DE VIE OU TOUT CHANGEMENT À LA SUITE DE QUELQUE CHOSE QUE VOUS AVEZ LU SUR GoVeganWay.com AVANT DE CONSULTER UN PRATICIEN MÉDICAL AGRÉÉ.
En cas d'urgence médicale, appelez immédiatement un médecin ou le 911. GoVeganWay.com ne recommande ni n'approuve aucun groupe, organisation, test, médecin, produit, procédure, opinion ou autre information spécifique pouvant être mentionné à l'intérieur.
Choix de l'éditeur -
Milos Pokimica est rédacteur spécialisé dans la santé et la nutrition et conseiller en sciences nutritionnelles. Auteur d'une série de livres Devenir vegetarien ? Examen des sciences, il exploite également le site Web de santé naturelle GoVeganWay.com
Derniers articles –
Top Des Nouvelles Sur la Santé - ScienceDaily
- Scientists boosted one protein and aging mice became stronger and healthierle mai 19, 2026
Scientists have identified a protein that appears to put the brakes on the chronic inflammation linked to aging. Older mice with boosted levels of the protein were stronger, more energetic, and had healthier bones than untreated mice. Researchers say the findings could eventually lead to therapies that help people stay healthier and more independent later in life.
- People who lost the most weight on Ozempic saw huge health benefitsle mai 19, 2026
People who lost significant weight while taking Ozempic, Wegovy, Mounjaro, or Saxenda had sharply lower risks of major obesity-related health problems, including sleep apnea and kidney disease. Those who gained weight instead faced higher risks — especially for heart failure — even though many patients discontinued the medications within a year.
- Scientists found a smarter Mediterranean diet that slashes diabetes risk by 31%le mai 19, 2026
A large European study revealed that a lower-calorie Mediterranean diet paired with exercise and coaching dramatically reduced the risk of type 2 diabetes. Participants who made these lifestyle changes were 31% less likely to develop the disease over six years. They also lost more weight and trimmed their waistlines compared to those following a standard Mediterranean diet alone.
- Hidden sugar patterns on human cells could reveal cancer earlyle mai 18, 2026
Scientists have uncovered a hidden “sugar code” on the surface of human cells that could transform how diseases are detected. Using an advanced imaging technique called Glycan Atlasing, researchers at the Max Planck Institute mapped the tiny sugar structures coating cells and discovered that these patterns shift depending on what the cell is doing. Immune cells changed their sugar layouts when activated, and cancerous tissues displayed distinct surface signatures compared to healthy tissue.
- Eating grapes daily could unlock powerful skin protectionle mai 18, 2026
Scientists discovered that eating grapes can actually change how your skin behaves at the genetic level. After just two weeks of daily grape consumption, volunteers showed signs of improved skin protection and reduced oxidative stress from UV exposure. Researchers say the effects appear widespread, even though every person’s genes responded a little differently.
- This popular fermented food may help flush microplastics from the bodyle mai 18, 2026
Scientists in South Korea have discovered that a probiotic bacterium found in kimchi may help the body flush out tiny plastic particles before they can build up in organs. In lab tests, the kimchi-derived microbe clung tightly to nanoplastics even under conditions designed to mimic the human intestine, where other bacteria quickly lost their grip.
- Scientists think they’ve cracked the mystery of human right-handednessle mai 18, 2026
A new study suggests humans became overwhelmingly right-handed because of two major evolutionary shifts: walking on two legs and developing much larger brains. Researchers found that as human ancestors evolved, their right-hand preference steadily intensified — transforming a mild tendency into one of humanity’s most distinctive traits.
PubMed, #régime-vegan –
- Flaxseed Mucilage as a Functional Egg Replacer in the Preparation of Mayonnaise: Stability, Physicochemical, and Sensory Propertiesle mai 15, 2026
Mayonnaise is a widely consumed food dressing worldwide. Traditionally, it is prepared by emulsification of oil with egg yolk. However, the use of eggs is limited due to their cholesterol-rich content, allergenicity, and high price, as well as the vegan and healthy dietary preferences of consumers. Flaxseed mucilage, as a natural hydrocolloid gum, exhibits comparable functional properties, especially emulsifying activity, to commercial gums. In this study, egg yolk in mayonnaise was […]
- Severe Hypocalcaemia with Elevated PTH and Normal Vitamin D: A Diagnostic Pitfall due to Chronic Negative Calcium Balance in a Vegan Patientle mai 14, 2026
CONCLUSION: A chronic negative calcium balance is an under-recognised cause of secondary hyperparathyroidism. Measurement of urinary calcium is a key diagnostic tool in these patients.
- Plant-based diets for human health with implications for cardiometabolic health, gut microbiome, and nutritional adequacyle mai 14, 2026
Plant-based diets have gained considerable interest in recent times due to their perceived health and environmental benefits. However, the term “plant-based diet” refers to a broad range of diets with a wide range of differences in food quality and nutritional content. This article aims to summarize the available evidence regarding the health and environmental impacts of plant-based diets, including new trends and issues. Epidemiological studies, RCTs, and life cycle assessment studies were…
- The Role of Microbiome and Diet on Disease Activity and Immune-Inflammatory Status in Rheumatoid Arthritisle mai 13, 2026
Rheumatoid arthritis (RA) is a chronic inflammatory disease of autoimmune background and unknown etiology. The importance of genetic factors in RA development is well-established. Environmental factors have also been extensively researched in relation to risk of RA and managing its symptoms. Smoking, physical activity, diet, and gut microbiota are considered to be the most essential modifiable factors in RA. Among dietary interventions, the most researched is Mediterranean diet, […]
- Comparative development of volatile-oriented multi-SPME and derivatisation-based GC×GC-TOFMS workflows for non-targeted faecal metabolomicsle mai 13, 2026
Gas chromatography-mass spectrometry (GC-MS) remains a key technique in metabolomics, yet most workflows rely on chemical derivatisation to enable the analysis of non-volatile metabolites. Although derivatisation broadens metabolite coverage, it increases sample preparation time and may introduce additional analytical variabilities. In contrast, solid-phase microextraction (SPME) enables rapid, solvent-free sampling of volatile and semi-volatile compounds, representing an attractive […]
Messages aléatoires –
Postes en vedette -
Dernières Nouvelles de PubMed, #alimentation végétale –
- The Plant Compound Sulforaphane Attenuates Induction of Cytokines and Other Early Activation Events in Jurkat Cellspar Qi Fu le mai 19, 2026
Sulforaphane (SFN), a bioactive isothiocyanate found in cruciferous vegetables, has gained considerable interest for its anti-inflammatory and immunomodulatory properties. Previous work in our lab demonstrated that tert-butylhydroquinone (tBHQ), a common food preservative and synthetic antioxidant, suppresses early T cell activation events, including production of interleukin-2 (IL-2) and other cytokines, cell proliferation and induction of interleukin-2 receptor alpha (CD25) and other […]
- From Single Conventional Regression to Ensemble Modeling: Relative Importance of the Healthy Eating Index-2015 Components in Relation to Adverse Pregnancy Outcomespar Julie M Petersen le mai 18, 2026
The Healthy Eating Index (HEI) is widely used to assess diet quality, but certain contexts (e.g., pregnancy) may benefit from tailored versions. We evaluated whether the HEI’s current approach of assigning approximately equal weights to all components to compute the total score is appropriate when studying diet quality around conception. Data were from a U.S. prospective cohort of individuals who had not delivered a previous pregnancy past 20 weeks’ gestation (2010-2013, n=7882). Usual […]
- Adherence to the Mediterranean diet among adolescents: A comparison of two versions of KIDMEDpar Imane Haddou le mai 18, 2026
CONCLUSIONS: The UV of KIDMED in light of current nutritional recommendations, leads to a more demanding assessment of eating behaviors and better identification of at-risk dietary patterns in adolescents, without altering the OV structure.
- (Poly)phenol profiles of plant-based diets assessed through dietary intake and urinary biomarkerspar E Casas-Albertos le mai 18, 2026
(Poly)phenols are bioactive compounds widely present in plant-based foods. The aim was to explore differences in (poly)phenols based on dietary intake and urinary measurements among omnivores and different types of plant-based diets (PBDs). A total of 792 participants completed a 175-item food frequency questionnaire; 200 (51% PBD followers) provided first-morning urine samples. The Phenol-Explorer database was used to estimate dietary (poly)phenol intake. Food contributions to total…
- Associations of plant based dietary intake and physical activity with depression symptoms in older adults aged 65 years and above in longevity areas in Chinapar X Meng le mai 18, 2026
Objective: To investigate the associations of plant based dietary intake and physical activity with depression symptoms in old adults aged ≥65 years in longevity areas in China. Methods: Based on cross-sectional data from the Healthy Ageing and Biomarkers Cohort Study conducted in 2021. Information about demographic characteristics, lifestyles, and psychological characteristics of the old adults were collected. Plant based dietary index (PDI) was obtained and calculated according to the […]
- Grapholita molesta V-ATPase D acts as a susceptibility determinant of larvae to Bt Cry2Ab toxinpar Yanshen Fu le mai 17, 2026
Grapholita molesta is a globally significant and destructive pest, particularly notorious for its impact on the fruit industry. Cry2Ab is a crucial alternative Bt protein used to manage the resistance to Cry1A toxins, and it is effective against a range of Lepidoptera pests. Previous studies have confirmed that subunits A, B, C, and E of vacuolar H^(+)-ATPase are involved in the insecticidal efficacy of Bt. Based on the previous LC-MS/MS results, V-ATPase D was selected in this study to […]